Необычные свойства воды давно являются объектом пристального изучения учёных. Десять лет назад выяснилось, что внутри нанотрубок диаметром менее 2,5 нм вода не замерзает, а продолжает течь даже при температурах, близких к абсолютном нулю (−273,15°C). Странности на этом не заканчиваются.
Фазовые переходы воды со сменой агрегатного состояния внутри углеродных нанотрубок явно не вписываются в стандартную теорию термодинамики. Это касается не только точки замерзания, но и точки кипения. Как известно, при нормальном атмосферном давлении температура кипения воды составляет около 100°C. При увеличении давления в ёмкости температура кипения увеличивается - этот принцип используют скороварки, чтобы быстрее приготовить пищу. И наоборот, температуру кипения воды можно снизить, уменьшив давление. Например, в горах на высоте 5 км приготовить некоторые продукты в принципе невозможно, потому что там температура кипения воды составляет всего лишь 83°C из-за пониженного атмосферного давления.
Учёным известно также, что температура фазовых переходов воды зависит также от формы и размера сосуда. При неизменности давления с помощью объёма сосуда можно сдвинуть точку кипения или точку замерзания примерно на 10°C. Но в углеродных нанотрубках всё становится с ног на голову. Как уже упоминалось, вода сохраняет там жидкое состояние при температурах, близких к абсолютному нулю. Сейчас учёные из Массачусетского технологического института (МТИ) ещё один интересный феномен - фазовый переход в твёрдое состояние (ледяные нанотрубки) при высокой температуре, когда в нормальных условиях вода должна испаряться.
Этот феномен обнаружен в 2001 году группой японских и американских учёных. Ледяные нанотрубки представляют особенный интерес, потому что они образуются при высокой температуре и могут быть использованы в различных электронных наноустройствах, в том числе в газовых нанотурбинах , нанодатчиках потока и высокопоточных мембранах. Более того, способность воды замерзать в ледяные нанотрубки при температурах гораздо выше 0°C делает возможным использование ледяных нанотрубок в системах теплообмена . Были получены экспериментальные подтверждения такого использования, но до сих пор не были известны и изучены точные размеры и параметры углеродных нанотрубок, которые необходимы для затвердения воды при комнатной температуре и выше.
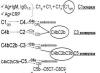
До настоящего времени большинство экспериментов с фазовым переходом воды в углеродных нанотрубках были ограничены симуляциями молекулярной динамики на компьютере, а не реальными физическими опытами. В результате симуляции выяснилось, что свойства воды сильно зависят от диаметра углеродной нанотрубки. Например, в порах диаметром 0,8−1,0 нм вода хорошо стабилизируется в парообразном состоянии, а где-то между диаметрами трубки 1,1 и 1,2 нм симуляции показывают стабилизацию в форме льда, то есть в твёрдом виде. Затем при увеличении диаметра свыше 1,4 нм опять наступает стабилизация в жидкой форме. Всё это очень интересно - и поэтому в МТИ разработали методологию физических опытов для проверки свойств воды в углеродных нанотрубках диаметром от 1,05 до 1,52 нм с одиночными и двойными стенками. Авторы эксперимента также разработали технику мониторинга воды в нанотрубках с помощью рамановской спектроскопии (радиальные колебания, RBM).

Экспериментальная установка для выращивания нанотрубок и заполнения их водой (почему гидрофобные нанотрубки пропускают внутрь воду - учёные тоже не до конца понимают); компьютерные модели однослойных и двухслойных нанотрубок для эксперимента; результаты рамановской спектроскопии
Эксперименты показали, что на некоторых диаметрах нанотрубок вода переходит в твёрдое агрегатное состояние при температурах выше 100°C. Максимально зарегистрированная температура фазового перехода составляет от 105°C до 151°C (точнее измерить не удалось) с диаметром однослойной нанотрубки 1,05 нм. Это гораздо выше параметров, которые предсказывала теория . В некоторых случаях реальная точка замерзания оказалась почти на 100°C выше, чем предсказывала теория. Впервые опыты был проведён в реальных лабораторных условиях - как выяснилось, не зря. Никто не ожидал настолько большой разницы в свойствах воды в нанотрубках диаметром 1,05 и 1,06 нм.

Голубой цвет на диаграмме - твёрдое состояние воды, зелёный - жидкое состояние, красный - пустые нанотрубки (dry state)
После прохода через точку замерзания учёные опустили температуру и вернули воду в жидкое состояние, доказав обратимость процесса. В нанотрубках диаметром 1,06 нм лёд таял при температуре 87−117°С, в нанотрубках 1,44 и 1,52 нм точка замерзания находится между 15−49°С и 3−30°С, соответственно.
Нанолёд обладает интересным сочетанием электрических и тепловых свойств. Наличие льда, который не тает при температуре до +151°С, может заинтересовать инженеров и конструкторов. При комнатной температуре такой лёд будет абсолютно стабильным, его вполне можно использовать как провода в электронике и других приборах (вода -
Если лед поместить в сосуд и поставить его над работающей горелкой, сосуд нагреется и лед начнет таять. Однако до тех пор, пока весь лед не превратится в жидкость, температура воды не поднимется выше 0°С (32°F), вне зависимости от степени разогрева плиты. Это происходит из-за того, что вся подводимая ко льду теплота идет на преодоление физических сил, связывающих между собой его молекулы.
У льда молекулы воды удерживаются вместе межмолекулярными связями, формирующимися между атомом водорода (показан синим цветом) одной молекулы и атомом кислорода (показан красным цветом) другой. Результирующая гексагональная кристаллическая структура имеет довольно высокую прочность. При 0°С молекулы движутся настолько быстро, что связи ослабевают. Часть межмолекулярных связей разрывается, позволяя молекулам воды покидать лед с образованием жидкости. Такой процесс называется фазовым переходом (вода переходит из твердой фазы в жидкую), а температура, при которой он протекает, называется точкой плавления.
Для разрушения связей, позволяющих воде находиться в твердом состоянии, необходима энергия, причем в очень большом количестве, поэтому вся теплота, выделяемая горелкой, идет на разрывание этих связей, а не на увеличение температуры льда. Теплота, необходимая для завершения описанного выше фазового превращения, называется скрытой теплотой плавления или теплотой фазового перехода, так как эта теплота не приводит к росту температуры. Только после того, как последние связи будут разрушены и весь лед расплавится, температура воды начнет увеличиваться и станет выше 0°С.
Как происходит таяние льда
- У льда молекулы воды движутся так медленно, что всегда сохраняют связь друг с другом, образуя твердое тело. Когда ко льду подводится теплота (на рисунке справа показана в виде желтых шариков), молекулы воды приобретают дополнительную энергию и движутся быстрее, однако все еще связанные вместе в виде льда.
- Если подвод теплоты продолжается, молекулы воды, находящиеся на поверхности льда, увеличивают скорость своих колебательных движений, разрывая межмолекулярные связи, удерживавшие их раньше на месте. Эти молекулы покидают лед и образуют жидкую фазу воды. Дальнейший подвод теплоты приводит к разрушению оставшихся межмолекулярных связей и постепенному таянию льда.
- Продолжающийся подвод теплоты в конце концов дает последним из молекул замерзшей воды достаточно энергии для преодоления межмолекулярных связей, удерживавших их вместе в виде льда. Вся вода теперь стала жидкостью.

Лед, вода и температура

При подводе ко льду теплоты (рисунок слева) сначала увеличивается его температура. Однако при 0°С (32°F) рост температуры прекращается и наступает фазовый переход: лед начинает таять. Как показывает голубая кривая на графике, дополнительный подвод теплоты приводит к дальнейшему таянию льда, не увеличивая температуру воды. Только после того как весь лед перейдет в жидкое состояние (рисунок над текстом), дополнительный подвод теплоты приводит к увеличению температуры воды.
Край промоины влечет к себе рыболова-подледника, хотя опасность того, что вблизи открытой воды лед окажется явно непрочным, присутствует всегда. Условиями безопасного передвижения по льду являются знание рисков и надлежащее снаряжение. Приведенные здесь сведения обязательно помогут обеспечить Вашу безопасность.
Осенью первыми покрываются льдом мелкие озерки, а затем – прибрежные воды и неглубокие заливы озер. Замерзание водоемов происходит от берегов к плесам. Наиболее глубокие места могут оставаться не замерзшими еще месяц-два после того, как прибрежные участки уже покрылись льдом, поскольку большая водная масса остывает медленнее.
В море затягивание льдом архипелагов и открытых морских участков зависит как от продолжительности морозных периодов, так и от ветра и течений. В открытом море ледовый покров «живет» на протяжении всей зимы. Вследствие перемещения и растрескивания ледяных полей, между льдинами могут возникать коридоры практически лишенные льда, в которые рыболов – блеснильщик и рискует провалиться.
Факторы влияющие на прочность льда
Сначала лед образуется неравномерно, но по мере дальнейшего остывания воды он нарастает в спокойную погоду со скоростью 2,5 мм в сутки на один градус мороза. Если, например, температура воздуха составляет – 4 градуса, то можно сказать, что за сутки может образоваться лед толщиной в сантиметр.
Приведем для наглядности таблицу прироста льда, в зависимости от температуры окружающей среды.
| Температура воздуха | < 10 см | 10-20 см | 20-40 см |
|---|---|---|---|
| Прирост за сутки, см | Прирост за сутки, см | Прирост за сутки, см | |
| -5 | 4 | 1,5 | 0,5 |
| -10 | 6 | 3 | 1,5 |
| -15 | 8 | 4 | 2 |
| -20 | 9 | 6 | 3 |
Мнение эксперта
Александр Петрович
участник Чемпионата России по ловле на поплавочную удочку
Стоит учесть, что мутная или солоноватая вода замерзает хуже чистой и пресной, и, соответственно, прирост толщины льда происходит медленнее.
Большое влияние оказывают и другие факторы:
- глубина водоема;
- сила течения;
- толщина снежного покрова;
- сила ветра и т.п.
Мощность ледяного покрова обычно увеличивается со столь прямой зависимостью на небольших мелких озерках. В крупных озерах, не говоря уж о море, большая масса воды на глубоких участках замедляет замерзание и скорость нарастания мощности льда невозможно определить с берега.
Снег, ложащийся на прозрачный, толщиной один – два сантиметра ледок – это еще одна опасность для рыболова – блеснильщика. Уже небольшой слой снега замедляет нарастание льда или даже прекращает его полностью.
Если же снега наметет на первый лед как следует, то мощный снежный покров прижимает лед к поверхности воды. Через трещины на поверхность льда вытекает вода. Передвижение по льду при этом становится трудным и весьма опасным, поскольку лед может проломиться или даже растаять в воде под снегом.
Вода, вытекшая на лед, впитывается в снег, образуя слякоть. На этих слякотных участках после их замерзания возникают наледи. Несущая способность ноздреватого и хрупкого льда на участках наледи наполовину меньше, чем у обычного.
Разница температур между верхней и нижней поверхностью льда в особенности при резком похолодании обусловливает неравномерное увеличение ледяного покрова и образование полыней. Вода поднимается через полыньи на лед и замерзает. При потеплении замерзшая в полыньях вода препятствует расширению льдин до их исходного размера. В ледовом покрове возникают внутренние напряжения, которые выталкивают лёд на берег, вследствие чего создаются нагромождения льда, торосы.
Лечение водой
Кувшинные фильтры, картриджи
Вода при 4°С
Вопрос:
При 4 °С вода имеет максимальную плотность. Почему? почему вода на дне водоема именно при этой температуре? заранее спс. Саша
Ответ:
Уважаемый, Александр!
Вода - одно из самых загадочных веществ нашей планеты. Будучи нормальным мономолекулярным соединением, она должна была бы кипеть при + 70°C, а замерзать почти при -100°C. В отличие от всех остальных жидкостей, вода при затвердевании уменьшает свой вес. Максимальная плотность воды наблюдается при +4°C. Этот факт чрезвычайно важен для биосферы. В результате лед образуется на поверхности водоемов, не давая им промерзать до дна, и, тем самым, не давая погибнуть рыбам и прочим представителям водной фауны в зимнее время.
Поверхностное натяжение чистой воды больше, чем у любой другой жидкости, кроме ртути. У абсолютно чистой воды поверхностное натяжение таково, что по ней можно было бы кататься на коньках. Наличие примесей резко снижает величину поверхностного натяжения воды. Одна из "странностей" воды в том, что это вещество - единственное на Земле - всегда выступает в трех фазах - жидком, твердом и газообразном.
Молекула воды имеет угловое строение; входящие в ее состав ядра образуют равнобедренный треугольник, в основании которого находятся два протона, а в вершине - ядро атома кислорода. Межъядерные расстояния О-Н близки к 0,1 нм, расстояние между ядрами атомов водорода равно примерно 0,15 нм. Из восьми электронов, составляющих внешний электронный слой атома кислорода в молекуле воды, две электронные пары образуют ковалентные связи О-Н, а остальные четыре электрона представляют собой две неподеленные электронные пары. Таким образом, молекула воды представляет собой маленький диполь, содержащий положительный и отрицательный заряды на полюсах. Так как масса и заряд ядра кислорода больше чем у ядер водорода, то электронное облако стягивается в сторону кислородного ядра. При этом ядра водорода “оголяются”. Таким образом, электронное облако имеет неоднородную плотность. Около ядер водорода имеется недостаток электронной плотности, а на противоположной стороне молекулы, около ядра кислорода, наблюдается избыток электронной плотности. Именно такая структура и определяет полярность молекулы воды. Если соединить прямыми линиями эпицентры положительных и отрицательных зарядов получится объемная геометрическая фигура - правильный тетраэдр.
Молекулярная масса парообразной воды равна 18 и отвечает ее простейшей формуле. Однако молекулярная масса жидкой воды, определяемая путем изучения ее растворов в других растворителях, оказывается более, высокой. Это свидетельствует о том, что в жидкой воде происходит ассоциация молекул, т.е. соединение их в более сложные агрегаты. Такой вывод подтверждается и аномально высокими значениями температур плавления и кипения воды. Ассоциация молекул воды вызвана образованием между ними водородных связей.
Благодаря наличию водородных связей каждая молекула воды образует водородную связь с 4-мя соседними молекулами, образуя ажурный сетчатый каркас в молекуле льда. Однако, в жидком состоянии вода – неупорядоченная жидкость; эти водородные связи - спонтанные, короткоживущие, быстро рвутся и образуются вновь. Всё это приводит к неоднородности в структуре воды.
Водородные связи между молекулами воды
То, что вода неоднородна по своему составу, было установлено давно. С давних пор известно, что лёд плавает на поверхности воды, то есть плотность кристаллического льда меньше, чем плотность жидкости. Почти у всех остальных веществ кристалл плотнее жидкой фазы. К тому же и после плавления при повышении температуры плотность воды продолжает увеличиваться и достигает максимума при 4°C. Менее известна аномалия сжимаемости воды: при нагреве от точки плавления вплоть до 40°C она уменьшается, а потом увеличивается. Теплоёмкость воды тоже зависит от температуры немонотонно. Кроме того, при температуре ниже 30°C с увеличением давления от атмосферного до 0,2 ГПа вязкость воды уменьшается, а коэффициент самодиффузии - параметр, который определяет скорость перемещения молекул воды относительно друг друга растёт. Для других жидкостей зависимость обратная, и почти нигде не бывает, чтобы какой-то важный параметр вёл себя не монотонно, т.е. сначала рос, а после прохождения критического значения температуры или давления уменьшался. Возникло предположение, что на самом деле вода - это не единая жидкость, а смесь двух компонентов, которые различаются свойствами, например плотностью и вязкостью, а следовательно, и структурой. Такие идеи стали возникать в конце XIX века, когда накопилось много данных об аномалиях воды.
Сейчас наукой доказано, что особенности физических свойств воды и многочисленные короткоживущие водородные связи между соседними атомами водорода и кислорода в молекуле воды создают благоприятные возможности для образования особых структур-ассоциатов (кластеров), воспринимающих, хранящих и передающих самую различную информацию.
Структурной единицей такой воды является кластер, состоящий из клатратов, природа которых обусловлена дальними кулоновскими силами. В структуре кластров закодирована информация о взаимодействиях, имевших место с данными молекулами воды. В водных кластерах за счёт взаимодействия между ковалентными и водородными связями между атомами кислорода и атомами водорода может происходить миграция протона (Н+) по эстафетному механизму, приводящие к делокализации протона в пределах кластера.
Вода, состоящая из множества кластеров различных типов, образует иерархическую пространственную жидкокристаллическую структуру, которая может воспринимать и хранить огромные объемы информации.
Лёд – кристаллическая модификация воды. По последним данным лёд имеет 14 структурных модификаций. Среди них есть и кристаллические (их большинство) и аморфные модификации, но все они отличаются друг от друга взаимным расположением молекул воды и свойствами. Правда, все, кроме привычного нам льда, кристаллизующего в гексагональной сингонии, образуются в условиях экзотических - при очень низких температурах и высоких давлениях, когда углы водородных связей в молекуле воды изменяются и образуются системы, отличные от гексагональной. Такие условия напоминают космические и не встречаются на Земле. Например, при температуре ниже –110 °С водяные пары выпадают на металлической пластине в виде октаэдров и кубиков размером в несколько нанометров - это так называемый кубический лед. Если температура чуть выше –110 °С, а концентрация пара очень мала, на пластине формируется слой исключительно плотного аморфного льда.
Наиболее изученным является лёд I-й природной модификации. Лёд встречается в природе в виде льда (материкового, плавающего, подземного и т.д.), а также в виде снега, инея и т.д. Он распространён во всех областях обитания человека. Собираясь в огромных количествах, снег и лед образуют особые структуры с принципиально иными, нежели у отдельных кристаллов или снежинок, свойствами. Ледники, ледяные покровы, вечная мерзлота, сезонный снежный покров существенно влияют на климат больших регионов и планеты в целом: даже те, кто никогда не видел снега, чувствуют на себе дыхание его масс, скопившихся на полюсах Земли, например, в виде многолетних колебаний уровня Мирового океана. Лед имеет столь большое значение для облика нашей планеты и комфортного обитания на ней живых существ, что ученые отвели для него особую среду - криосферу, которая простирает свои владения высоко в атмосферу и глубоко в земную кору.
Две последние модификации льда - XIII и XIV - открыли ученые из Оксфорда совсем недавно, в 2006 году. Предположение о том, что должны существовать кристаллы льда с моноклинной и ромбической решетками, было трудно подтвердить: вязкость воды при температуре –160°С очень высока, и собраться вместе молекулам чистой переохлажденной воды в таком количестве, чтобы образовался зародыш кристалла, трудно. Этого удалось достичь с помощью катализатора - соляной кислоты, которая повысила подвижность молекул воды при низких температурах. В земной природе подобные модификации льда образовываться не могут, но они могут встречаться на замерзших спутниках других планет.
Табл. Некоторые известные модификации льда
Примечание. 1 A=10 -10 м.
Разгадка структуры льда заключается в строении его молекулы. Кристаллы всех модификаций льда построены из молекул воды H 2 O, соединённых водородными связями в трёхмерный каркас, аналогичный структуре алмаза. Именно в связи с тем, что лёд имеет такую высокорегулярную сетчатую структуру и связи с низким координационным числом лёд имеет невысокую плотность.
Рис. Структура алмаза
Рис.. Структура льда.
Каждая молекула в структуре льда участвует в 4 таких связях, направленных к вершинам тетраэдра. При взаимодействии протона одной молекулы с парой неподеленных электронов кислорода другой молекулы возникает водородная связь, менее сильная, чем связь внутримолекулярная, но достаточно могущественная, чтобы удерживать рядом соседние молекулы воды. Каждая молекула может одновременно образовывать четыре водородные связи с другими молекулами под строго определенными углами, равными 109°28", направленных к вершинам тетраэдра, которые не позволяют при замерзании создавать плотную структуру. При этом в структурах льда I, Ic, VII и VIII этот тетраэдр правильный. В структурах льда II, III, V и VI тетраэдры заметно искажены. В структурах льда VI, VII и VIII можно выделить 2 взаимоперекрещивающиеся системы водородных связей. Этот невидимый каркас из водородных связей располагает молекулы в виде сетчатой сетки, по структуре напоминающей соты с полыми каналами. Если лед нагреть, сетчатая структура разрушится: молекулы воды начинают проваливаться в пустоты сетки, приводя к более плотной структуре жидкости, - именно поэтому вода тяжелее льда.
Лед, который образуется при атмосферном давлении и плавится при 0 °С, - самое привычное, но всё же до конца не понятное вещество. Многое в его структуре и свойствах выглядит необычно. В узлах кристаллической решетки льда атомы кислорода выстроены упорядоченно, образуя правильные шестиугольники, а атомы водорода занимают самые разные положения вдоль связей. Поэтому возможны 6 эквивалентных ориентаций молекул воды относительно их соседей. Часть из них исключается, поскольку нахождение одновременно 2 протонов на одной водородной связи маловероятно, но остаётся достаточная неопределённость в ориентации молекул воды. Такое поведение атомов нетипично, поскольку в твердом веществе все подчиняются одному закону: либо все атомы расположены упорядоченно, и тогда это - кристалл, либо случайно, и тогда это - аморфное вещество. Такая необычная структура может реализоваться в большинстве модификаций льда - I, III, V, VI и VII (и по-видимому в Ic), а в структуре льда II, VIII и IX молекулы воды ориентационно упорядочены. По выражению Дж. Бернала лёд кристалличен в отношении атомов кислорода и стеклообразен в отношении атомов водорода.
Значение льда трудно недооценить. Лёд оказывает большое влияние на условия обитания и жизнедеятельности растений и животных, на разные виды хозяйственной деятельности человека. Покрывая воду сверху, лед играет в природе роль своего рода плавучего экрана, защищающего реки и водоемы от дальнейшего замерзания и сохраняющего жизнь подводному миру. Если бы плотность воды увеличивалась при замерзании, лед оказался бы тяжелее воды и начал тонуть, что привело бы к гибели всех живых существ в реках, озерах и океанах, которые замерзли бы целиком, превратившись в глыбы льда, а Земля стала ледяной пустыней, что неизбежно привело бы к гибели всего живого.
В связи с широким распространением воды и льда на Земле отличие свойств льда от свойств других веществ играет важную роль в природных процессах. Вследствие меньшей, чем у воды, плотности лёд образует на поверхности воды плавучий покров, предохраняющий реки и водоёмы от донного замерзания. Зависимость между скоростью течения и напряжением у поликристаллического льда гиперболическая; при приближённом описании её степенным уравнением показатель степени увеличивается по мере роста напряжения.
Кроме того, скорость течения льда прямо пропорциональна энергии активации и обратно пропорциональна абсолютной температуре, так что с понижением температуры лёд приближается по своим свойствам к абсолютно твёрдому телу. В среднем при близкой к таянию температуре текучесть льда в 106 раз выше, чем у горных пород. Благодаря своей текучести лёд не накопляется в одном месте, а в виде ледников постоянно перемещается.
К другим необычным свойствам льда относят и генерацию электромагнитного излучения его растущими кристаллами. Известно, что большинство растворенных в воде примесей не передается льду, когда он начинает расти; они вымораживается. Поэтому даже на самой грязной луже пленка льда чистая и прозрачная. При этом примеси скапливаются на границе твердой и жидкой сред, в виде двух слоев электрических зарядов разного знака, которые вызывают значительную разность потенциалов.
Заряженный слой примесей перемещается вместе с нижней границей молодого льда и излучает электромагнитные волны. Благодаря этому процесс кристаллизации можно наблюдать в деталях. Так, кристалл, растущий в длину в виде иголки, излучает иначе, чем покрывающийся боковыми отростками, а излучение растущих зерен отличается от того, что возникает, когда кристаллы трескаются. По форме, последовательности, частоте и амплитуде импульсов излучения можно определить, с какой скоростью замерзает лед и какая при этом получается ледовая структура.
Так почему же максимальная плотность воды наблюдается при +4°C? Дело в том, что при таянии льда его структура разрушается. Но и в жидкой воде сохраняются водородные связи между молекулами: образуются ассоциаты - обломки структур льда, - состоящих из большего или меньшего числа молекул воды.
Однако в отличит от льда каждый ассоциат существует очень короткое время: постоянно происходит разрушение одних и образование других агрегатов. В пустотах таких “ледяных” агрегатов могут размещаться одиночные молекулы воды; при этом упаковка молекул воды становится более плотной. Именно поэтому при таянии льда объем, занимаемый водой, уменьшается, а ее плотность возрастает.
Образование водородных связей приводит к такому расположению молекул воды, при котором они соприкасаются друг с другом своими разноименными полюсами. Молекулы образуют слои, причем каждая из них связана с тремя молекулами, принадлежащими к тому же слою, и с одной – из соседнего слоя. Структура льда принадлежит к наименее плотным структурам, в ней существуют пустоты, размеры наименее плотным структурам, в ней существуют пустоты, размеры которых несколько превышают размеры молекулы.
Вода при таянии льда сохраняет температуру 4 °С, пока не растает весь лёд. При этом специфика межмолекулярных взаимодействий, характерная для структуры льда, сохраняется и в талой воде при 4 0С, так как при плавлении кристалла льда разрушается только 15% всех водородных связей в молекуле. Поэтому присущая льду связь каждой молекулы воды с четырьмя соседними молекулами в значительной степени не нарушается, хотя и наблюдается бoльшая размытость кислородной каркасной решетки.
Поэтому вода при 4 0С отличается от обычной изобилием многомолекулярных кластеров, в которых в течение некоторого времени сохраняются рыхлые льдоподобные структуры. После таяния всего льда температура воды повышается и водородные связи внутри кластеров перестают противостоять возрастающим тепловым колебаниям атомов. Размеры кластеров изменяются, и поэтому начинают меняться свойства талой воды: диэлектрическая проницаемость приходит к своему равновесному состоянию через 15-20 минут, вязкость - через 3-6 суток. Биологическая активность такой талой воды спадает, по одним данным, приблизительно за 12-16 часов, по другим - за сутки. Физико-химические свойства талой воды самопроизвольно меняются во времени, приближаясь к свойствам обычной воды: она постепенно как бы "забывает" о том, что еще недавно была льдом.
Однако по мере нагревания воды, обломков структуры льда в ней становится все меньше, что приводит к дальнейшему повышению плотности воды. В интервале температур от 0 до 4°С этот эффект преобладает над тепловым расширением, так что плотность воды продолжает возрастать. Однако при нагревании выше 4°С преобладает влияние усиления теплового движения молекул и плотность воды снова уменьшается. Поэтому при 4°С вода обладает максимальной плотностью. При нагревании воды часть теплоты затрачивается на разрыв водородных связей (энергия разрыва водородной связи в воде составляет примерно 25 кДж/моль). Этим фактом и объясняется в частности, высокая теплоемкость воды.
Таким образом, увеличение плотности при плавлении, как и в случае плотных модификаций льда, объясняется искривлением водородных связей и отклонением углов между ними от тетраэдрических. Искривление связей увеличивается с ростом температуры и давления, что приводит к возрастанию плотности. С другой стороны, при нагревании средняя длина водородных связей становится больше, в результате чего плотность уменьшается. Совместное действие двух факторов объясняет наличие максимума плотности воды при 4 °С.
Плотность воды является одним из её важнейших свойств. Максимальную плотность пресная вода имеет при 4 С. При этой температуре один килограмм воды занимает минимальный объем. При понижении температуры от 4 0С до 0 С плотность воды уменьшается, т. е. вода с температурой 4 0С находится внизу как более плотная вода, а более холодная вола с низкой плотностью поднимается наверх, где и замерзает, превращаясь в лед. Понятно, почему не работает механизм конвекции: плотность нагреваемой сверху воды уменьшается, она не может опуститься вниз и отдать тепло льду. Плотность льда в свою очередь меньше плотности воды, поэтому лед плавает на поверхности, предохраняя воду от дальнейшего охлаждения.
Если бы ни аномалия плотности воды, т.е. при понижении температуры и при переходе из жидкого состояния в твердое плотность воды изменялась так же, как это происходит у подавляющего большинства веществ, то при приближении зимы поверхностные слои природных вод охлаждались. бы до 0°С и опускались на дно, освобождая место более теплым слоям, и так продолжалось бы до тех пор, пока вся масса водоема не приобрела бы температуру 0°С. Далее вода начинала бы замерзать, образующиеся льдины погружались бы на дно и водоем промерзал бы на всю его глубину. При этом формы жизни в воде были бы невозможны. Но так как наибольшей плотности вода достигает именно при 4 °С, то перемещение ее слоев, вызываемое охлаждением, заканчивается при достижении этой температуры. При дальнейшем понижении температуры охлажденный слой, обладающий меньшей плотностью, остается на поверхности, замерзает и тем самым защищает лежащие ниже слои от дальнейшего охлаждения и замерзания.
В отличие от пресной воды, морская вода при охлаждении ведет себя иначе. Замерзает она не при 0 0С, а при -1,8-2,1 0С - в зависимости от концентрации растворенных в ней солей. Имеет максимальную плотность не при + 4 0С, а при -3,5 0С. Таким образом, она превращается в лед, не достигая наибольшей плотности. Если вертикальное перемешивание в пресных водоемах прекращается при охлаждении всей массы воды до +4 0С, то в морской воде происходит даже при температуре ниже 0 0С. При этом процесс обмена между верхними и нижними слоями идет непрерывно.
С уважением,
к.х.н. О.В. Мосин
Доброго времени суток. Раньше где-то слышала, что лёд/снег тает при 4 градусах Цельсия. Но теперь не могу найти подтверждения этому факту. Можете дать пояснения, при какой температуре тает лёд в обычных условиях? А при каких условиях тает при 4 градусах Цельсия?
Парадокс плотности воды от +0 до +4 градусов в том что по
моему мнению вода H - O - H на самом деле физически несимметрична, но с химической стороны вроде - бы в норме.
Вроде - бы, но нет.
И это свойство несимметричности на самом деле есть во всех структурах и молекулах с изменением температуры как и в случае с водой.
Эффект Мпемба тоже выглядит необычно в моей температурной модели.
Друзья, это знания 8 класса средней школы, и не нам объяснять, почему вода - это диполь, или почему она замерзает при +4 С. Это вам должны были объяснить ещё в школе. Если не объяснили - вопрос легко находит ответ, стоит только открыть любой учебник или справочник.
Здесь мы стремимся привлечь более компетентную аудиторию, давайте держать соответствующие рамки и не опускаться ниже школьной программы по химии 8 класса, будем выше - раскрывать связи, закономерности и т.д. и т.п.
Друзья, подскажите как приготовить лед с повышенной температурой плавления? Например +15 градусов по Цельсию.
Среда нахождения и пространство обладает структурой. Эта структура есть динамическая решетка эфира. Называя ее "динамической", я подчеркиваю, что она находится в постоянной динамике, ее структурные сегменты (частицы эфироны) находятся в постоянном движении и вращении, называя ее "решеткой", я подчеркиваю, что она есть одно целое, среда, заполняющая все пространство, тот самый эфир, который искали. Та самая магнитная решетка, о которой говорил и говорит Крайон. Официальный научный элемент судит о структуре магнитного поля магнита визуализируя его с помощью метода Фарадея - железных опилок. Для времен Фарадея это было по истине гениальным решением - "увидеть структуру магнитного поля"... Но Фарадей так и не определился с вопросом - "либо силовые линии магнита принадлежат самому магниту, либо силовые линии принадлежат пространству, а магнит просто искривляет эти линии"... С тех пор прошло 200 лет и сегодня для изучения магнитного поля альтернативные ученые применяют магнитную жидкость, которая состоит из тех же самых опилок, но в жидком состоянии. Сегодня альтернативная наука уверенно заявляет: "силовые линии магнитного поля земли лишь искривляются посредством магнита, но не принадлежат ему"... Визуализируя структуру магнитного поля с помощью просто железных опилок, мы получаем двух мерное, ограниченное для изучения изображение, "рисунок", на листе бумаги. Но если визуализировать магнитное поле с помощью магнитной жидкости, мы получим трехмерное изображение этой структуры. Однако, официальная наука, видать из-за недостаточного государственного финансирования так и не смогла приобрести такую жидкость... Может сбросимся по копейке? Мне не жалко на такое дело. В итоге знания официальной науки о структуре магнитного поля остановились на уровне Фарадея и дальше не продвинулись. Да, появились датчики магнитного поля, которые несут некоторые характеристики и информацию о свойствах магнитного (электромагнитного) поля, но не о самом главном - структуре магнитного поля. Если вдруг, официальная наука решится на изучение структуры магнитного поля, она "откроет" для себя много разных и удивительных тайн природы.. Например, что пчелы делают свои соты круглыми, а шестигранниками они становятся уже без пчел под влиянием структуры магнитного поля земли! И главный вывод который их ожидает, что все физические взаимодействия в природе происходят посредством деформации (искривления) структуры магнитного поля вселенной или эфира. Начав изучать эту структуру, они поймут, что никаких "виртуальных частиц", "нейтрино", "фотонов", "гравитонов" не существует... Таким образом для ученых открывается огромная перспектива научного познания... Тот 100 летний "научный тормоз" будет преодолен за считанные годы для того, чтобы вывести Россию в лидеры научного руководства, всемирного "министра образования", который будет определять вектор развития прогресса нашей цивилизации.. Фарадей в своих трудах задавал себе вопрос... "принадлежат ли силовые линии магнита самому магниту или же силовые линии магнита принадлежат среде нахождения магнита"... Чтобы это выяснить, я срочно приобрел микроскоп, магнитную жидкость, настрогал сухих опилок, вооружился батарейками, блоками питания и катушками, обложил себя со всех сторон мультиметрами и всякими справочниками... Налил жидкость и увеличил ее в 20 раз... и я увидел там соты... и в одно мгновение я понял основной принцип.. Мгновенно я провел параллель с пчелиными сотами... потом я начал "применять" этот принцип к физическим явлениям, ячейкам Бенара, снежинкам, кристаллам, фигурам Хладини, ультразвуковой волне... базальтовым структурам, клеткам биологических объектов и прочим сотовым вещам в нашем мире... Сразу всплывают "Платоновы тела"... Теория динамической решетки эфира это перечень физических явлений и объяснение их смысла с позиции основного принципа их формирования, что перво основной средой их формирования является структура среды, т. Е. эфира. Вокруг любого тела на Земле существует "поле", только применительно к магниту мы говорим "магнитное поле", а применительно к живому объекту говорим "биологическое поле", а применительно к планете Земля говорим "гравитационное поле"... а применительно к звуковой волне говорим "звуковая волна"... Меняя его название мы лишь привязываем его к объекту, вокруг которого оно существует, но оно всюду одинаковое и имеет абсолютно одинаковую суть. Представьте себе много разных кораблей, ходящих по морю. Вы же не называете "вода этого корабля" или "вода другого корабля", так и поле для всех тел единое. Т. е. Нет множества разных полей и множества разных частиц, есть одно первородное поле но разного состояния и есть только одна единственная частица - эфирон, частица, которая может принимать бесконечное число своих структурных состояний, являя тем самым многообразие форм и геометрий окружающего нас мира. Большинство выводов электромагнетизма базируются на изначально ошибочном понимании и постулате из учебника о том, что якобы вокруг проводника образуется два поля: магнитное и электромагнитное. Сразу два поля! В то время как на самом деле вдоль и вокруг проводника магнитное поле земли существует всегда, структура которого под действием электричества искривляется в вихревое электромагнитное состояние. Т. е. Вокруг проводника не образуется два поля, а преобразуется одно и которое искривляется! Данный вывод не просто набор слов, а экспериментально подтвержденный факт. Что такое электрическое поле, что такое магнитное поле и что такое электромагнитное поле? Электрическое поле это электрический ток, просто мера изменения состояния частиц среды, как температура и давление - оно не материально. Т. е. Основной факт в том, что электричество или как его ошибочно называют "поле" - не материальная структура, а мера искривления (изменения состояния) материальной структуры Магнитного поле Земли. Электромагнитное поле это изменение структуры магнитного поля Земли в вихревое электромагнитное состояние. Даже тогда, когда Вы скажете: "вихревые токи Фуко", то под "вихревым" нельзя понимать сами "токи", а только материальную структуру электромагнитного поля, которая может быть вихревой и которая всегда снаружи по отношению к самому проводнику. Проводники, сердечники трансформаторов, да и вообще любая среда греются из-за силы трения материальных объектов - частиц эфиронов о материал (среду) сердечника или проводника, вызывая их нагрев. Магнитное поле преобразуется в вихревое электромагнитное состояние так: Структура магнитного поля - "относительно" неподвижные конуса, основание которых соты. Если систему некоторым образом возмутить (деформировать) т. Е. сообщить ей температуру, давление или электрический потенциал, соты преобразуются в вихревое состояние. Параметры вращения структуры, скорости, определяются параметрами самого возмущения. Например при силе тока 100 ампер и напряжении 1 вольт вихри практически стоят на месте их диаметр 0, 1 мм, но частота их вращения огромна. Поэтому они "трутся" создавая трение и образец нагревается. (индукционный нагрев). Повышая же напряжение системы мы будем увеличивать размер вихрей до образования так называемой "зоны ионизации", внутри которой могут зажигаться газовые лампы. Т. е. Меняя параметры возмущения мы будем менять скорость движения, частоту вращения, размер и геометрию самих вихрей. Вернемся к понятию "относительность", рассмотрев следующую аналогию. Известно, что при нагревании воды ее частицы начинают быстрее вращаться и двигаться. Вопрос: Частицы начали двигаться с нулевой скорости или они продолжили увеличивать свою скорость так, что для наблюдателя стало заметно отличие и он заключил: "частицы начали увеличивать скорость" ? Т. е. "нулевая скорость" или как говорят "нулевые колебания" - нулевые только относительно наблюдателя процесса, относительно скажем солнца они движутся и вращаются, но для наблюдателя они кажутся неподвижными! Т. е. Частицы наблюдателя и частицы спокойной воды колеблются с одинаковыми скоростями, и когда воду нагревают ее частицы не начинают двигаться, а лишь увеличивают свою скорость так, что становится заметно отличие. То же самое происходит и с частицами магнитного поля, которые в состоянии "нулевых колебаний" имеют сотовую структуру т. Е. нулевое, неподвижное относительно наблюдателя состояние. Как только мы сообщим возмущение системе, соты преобразуются в вихревые локальные структуры. Теория динамической решетки эфира имеет ясный, понятный и главное - визуализированный объект изучения - эфирон. Из экспериментов ясно, что он способен менять свою структуру, масштаб, частоту вращения, направление вращения, длину, ширину..
Красиво конечно, но, пока не подтверждено экспериментально - гуманоиды больше не наливать)
Да, кстати... Вода не замерзает при +4. Никогда.
Она даже при 0 замерзает не сразу, так как происходит процесс отдачи тепла в окружающую среду с градиентом понижения температуры поверхности, пропорциональным площади поверхности и глубине водоёма. И это имеет достаточно сложную характеристику переходного процесса. Но то, что при +4С вода имеет наибольшую плотность - да.