タングステンは金属の中で最も高融点です。 非金属元素の炭素だけがより高い融点を持っていますが、それは高圧でのみ液体の状態で存在します。 標準的な条件下では、タングステンは耐薬品性があります。
歴史と名前の由来
ウルフラミウムという名前は、16 世紀に知られていた鉱物のウルフラマイトからこの元素に移されました。 「オオカミの泡」と呼ばれます - 緯度。 スプマ・ルピまたはドイツ語。 ヴォルフ・ラーム。 この名前は、錫鉱石に付随するタングステンが錫の精錬を妨げ、錫をスラグの泡に変えたという事実によるものです(「羊をむさぼるオオカミのように錫をむさぼり食った」)。
物理的性質
タングステンは光沢のある明るい灰色の金属で、最も高い融点と沸点を持つことが証明されています(シーボーギウムはさらに耐火性が高いと考えられていますが、これまでのところ断言できません。シーボーギウムの寿命は非常に短いです)。 融点 - 3695 (3422 °C)、沸騰する温度は 5828 (5555 °C)。 純粋なタングステンの密度は 19.25 g/cm3 です。 常磁性特性 (磁化率 0.32⋅10 -9) を持ちます。 ブリネル硬度 488 kg/mm²、電気抵抗率 (20 °C) - 55⋅10 -9 Ohm m、2700 °C - 904⋅10 -9 Ohm m。 焼きなましたタングステンの音速は 4290 m/s です。
タングステンは、最も重く、最も硬く、最も高融点の金属の 1 つです。 純粋な形では、プラチナに似た銀白色の金属で、約 1600 °C の温度で容易に鍛造でき、細い糸に引き抜くことができます。 この金属は真空中で非常に安定です。
化学的性質
2 W + 4 H NO 3 + 10 H F ⟶ W F 6 + W O F 4 + 4 N O + 7 H 2 O (\displaystyle (\mathsf (2W+4HNO_(3)+10HF\longrightarrow WF_(6)+WOF_(4)+ 4NO\上矢印 +7H_(2)O)))酸化剤の存在下で溶融アルカリと反応します。
2 W + 4 Na O H + 3 O 2 ⟶ 2 Na 2 W O 4 + 2 H 2 O (\displaystyle (\mathsf (2W+4NaOH+3O_(2)\longrightarrow 2Na_(2)WO_(4)+2H_ (2)お))) W + 2 NaOH + 3 NaNO 3 ⟶ N a 2 W O 4 + 3 N a N O 2 + H 2 O (\displaystyle (\mathsf (W+2NaOH+3NaNO_(3)\longrightarrow Na_(2)WO_ (4)+3NaNO_(2)+H_(2)O)))この反応は最初はゆっくりと進みますが、400℃(酸素を伴う反応の場合は500℃)に達するとタングステンが自己発熱を始め、非常に激しく反応が進行し、多量の熱が発生します。
硝酸とフッ化水素酸の混合物に溶解し、ヘキサフルオロタングステン酸 H2 を形成します。 タングステン化合物の中で最も重要なものは、三酸化タングステンまたは無水タングステン、タングステン酸塩、一般式 Me 2 WO X の過酸化物化合物、およびハロゲン、硫黄、炭素を含む化合物です。 タングステン酸塩は、他の遷移金属を含むヘテロポリ化合物などのポリマーアニオンを形成する傾向があります。
応用
タングステンの主な用途は、冶金学における耐火材料の基礎としてです。
タングステン金属
タングステン接続
- 機械工学における金属および非金属構造材料の機械加工 (旋削、フライス加工、平削り、彫刻)、坑井掘削、および鉱業では、超硬合金および炭化タングステンをベースとした複合材料が広く使用されています (たとえば、コバルトマトリックス中の WC 結晶で構成され、ロシアで広く使用されているグレード - VK2、VK4、VK6、VK8、VK15、VK25、T5K10、T15K6、T30K4)、および炭化タングステン、炭化チタン、炭化タンタルの混合物 (TT)耐熱鋼のハツリ鍛造品やカンナ鍛造品、高強度材料のロータリーハンマードリルなど、特に困難な加工条件に適したグレードです。 鋼および鉄ベースの合金の合金元素(多くの場合モリブデンと一緒に)として広く使用されています。 「高速度」に分類され、文字 P で始まるマークが付いている高合金鋼には、ほとんどの場合タングステンが含まれています。
- 硫化タングステン WS 2 は高温 (500 °C まで) 潤滑剤として使用されます。
- 一部のタングステン化合物は触媒や顔料として使用されます。
- タングステン酸塩 (タングステン酸鉛、カドミウム、カルシウム) の単結晶は、核物理学および核医学において X 線およびその他の電離放射線のシンチレーション検出器として使用されます。
- ジテルル化タングステン WTe 2 は、熱エネルギーを電気エネルギー (熱起電力約 57 μV/K) に変換するために使用されます。
その他の用途
タングステン市場
金属タングステン(元素含有量約99%)の価格は、2010年末時点で1キログラム当たり約40~42ドルだったが、2011年5月には1キログラム当たり約53~55ドルとなった。 半製品は 58 米ドル (ロッド) から 168 米ドル (細ストリップ) まで。 2014 年のタングステン価格は 55 ドルから 57 ドルの範囲で変動しました。
生物学的役割
タングステンは重要な生物学的役割を果たしません。 一部の古細菌や細菌は、活性中心にタングステンを含む酵素を持っています。 深海の熱水噴出孔の周囲に生息する、偏性タングステン依存型の超好熱性古細菌が存在します。 酵素中のタングステンの存在は、初期古細菌の生理学的遺物と考えることができます。タングステンが生命の起源の初期段階で役割を果たしたという示唆があります。
天然タングステンは 5 つの同位体 (180 W - 0.12(1)%、182 W - 26.50(16)%、183 W - 14.31(4)%、184 W - 30.64(2) %、および 186 W - 28.43) の混合物で構成されています。 (19)%)。 天然タングステンの極めて弱い放射能(元素 1 グラム当たり年間約 2 回崩壊)は、180 W のα線放射能により発見され、その半減期は 1.8⋅10 18 年です。
注意事項
- マイケル・E・ヴィーザー、ノーマン・ホールデン、タイラー・B・コプレン、ジョン・K・ベルケ、マイケル・ベルグルンド、ウィリー・A・ブランド、ポール・ド・ビエーブル、マンフレッド・グルーニング、ロバート・D・ロス、ジュリス・メイヤ、平田隆文、トーマス・プロハスカ、ロニー・シェーンベルク、グレンダ・オコナー、トーマス・ワルチック、米田成、朱シャンクン。元素の原子量 2011 (IUPAC Technical Report) // 純粋化学と応用化学。 - 2013年。 - Vol. 85、いいえ。 5. - P. 1047-1078。 - DOI:10.1351/PAC-REP-13-03-02。
- タングステン: 物理的性質(英語) 。 WebElements。 2013 年 8 月 17 日に取得。
タングステン- 金属の中で最も耐火性が高い。 非金属元素である炭素だけがより高い融点を持っています。 標準条件下では耐薬品性があります。 ウルフラミウムという名前は、16 世紀に知られていた鉱物のウルフラマイトからこの元素に移されました。 緯度と呼ばれます。 Spuma lupi (「オオカミの泡」) またはドイツ語。 ウルフ・ラーム(「ウルフ・クリーム」、「ウルフ・クリーム」)。 この名前は、錫鉱石に含まれるタングステンが錫の精錬を妨げ、錫をスラグの泡に変えたという事実によるものです(「狼が羊を貪るように錫を貪る」)。
以下も参照してください。
構造
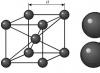
 タングステン結晶は体心立方格子を持っています。 低温のタングステン結晶は可塑性が低いという特徴があるため、粉末をプレスするプロセス中、基本的な形状とサイズは実質的に変化せず、粉末の圧縮は主に粒子の相対運動によって発生します。
タングステン結晶は体心立方格子を持っています。 低温のタングステン結晶は可塑性が低いという特徴があるため、粉末をプレスするプロセス中、基本的な形状とサイズは実質的に変化せず、粉末の圧縮は主に粒子の相対運動によって発生します。 体心立方タングステンセルでは、原子はセルの頂点と中心に位置します。 1 つの細胞には 2 つの原子があります。 bcc 構造は原子の最密充填ではありません。 コンパクト係数は 0.68 です。 タングステン宇宙群 Im3m。
プロパティ
 タングステンは光沢のある明るい灰色の金属で、最も高い融点と沸点を持つことが証明されています(シーボーギウムはさらに耐火性が高いと考えられていますが、これまでのところ断言できません。シーボーギウムの寿命は非常に短いです)。 融点 - 3695 K (3422 °C)、5828 K (5555 °C) で沸騰します。 純粋なタングステンの密度は 19.25 g/cm3 です。 常磁性特性(磁化率 0.32・10−9)を持っています。 ブリネル硬度 488 kg/mm²、電気抵抗率 (20 °C) - 55・10−9 Ohm・m、2700 °C - 904・10−9 Ohm・m。 焼きなましたタングステンの音速は 4290 m/s です。 常磁性です。
タングステンは光沢のある明るい灰色の金属で、最も高い融点と沸点を持つことが証明されています(シーボーギウムはさらに耐火性が高いと考えられていますが、これまでのところ断言できません。シーボーギウムの寿命は非常に短いです)。 融点 - 3695 K (3422 °C)、5828 K (5555 °C) で沸騰します。 純粋なタングステンの密度は 19.25 g/cm3 です。 常磁性特性(磁化率 0.32・10−9)を持っています。 ブリネル硬度 488 kg/mm²、電気抵抗率 (20 °C) - 55・10−9 Ohm・m、2700 °C - 904・10−9 Ohm・m。 焼きなましたタングステンの音速は 4290 m/s です。 常磁性です。
タングステンは、最も重く、最も硬く、最も高融点の金属の 1 つです。 純粋な形では、プラチナに似た銀白色の金属で、約 1600 °C の温度で容易に鍛造でき、細い糸に引き抜くことができます。
埋蔵量と生産量
 地殻のタングステン・クラークは(ヴィノグラドフによれば)1.3 g/t(地殻中の含有量の0.00013%)である。 岩石中の平均含有量、g / t:超塩基性 - 0.1、塩基性 - 0.7、中間 - 1.2、酸性 - 1.9。
地殻のタングステン・クラークは(ヴィノグラドフによれば)1.3 g/t(地殻中の含有量の0.00013%)である。 岩石中の平均含有量、g / t:超塩基性 - 0.1、塩基性 - 0.7、中間 - 1.2、酸性 - 1.9。
タングステンを得るプロセスは、鉱石精鉱から三酸化物WO 3 を分離し、その後、約700℃の温度で水素を用いて金属粉末に還元するというサブステージを経ます。 タングステンの融点は高いため、緻密な形状を得るには粉末冶金法が使用されます。得られた粉末をプレスし、水素雰囲気中で 1200 ~ 1300 °C の温度で焼結し、電流を流します。 金属は 3000 °C に加熱され、焼結が起こりモノリシック材料になります。 その後の精製と単結晶形態の取得には、ゾーンメルティングが使用されます。
起源
 タングステンは、自然界では主に三酸化タングステンWO 3 と鉄、マンガンまたはカルシウムの酸化物、場合によっては鉛、銅、トリウム、希土類元素との酸化複合化合物の形で存在します。 ウルフラマイト(鉄およびタングステン酸マンガン nFeWO 4 * mMnWO 4 - それぞれフェルベライトおよびヒュブネライト)および灰重石(タングステン酸カルシウム CaWO 4)は工業的に重要です。 タングステン鉱物は通常花崗岩に埋め込まれているため、平均タングステン濃度は 1 ~ 2% です。
タングステンは、自然界では主に三酸化タングステンWO 3 と鉄、マンガンまたはカルシウムの酸化物、場合によっては鉛、銅、トリウム、希土類元素との酸化複合化合物の形で存在します。 ウルフラマイト(鉄およびタングステン酸マンガン nFeWO 4 * mMnWO 4 - それぞれフェルベライトおよびヒュブネライト)および灰重石(タングステン酸カルシウム CaWO 4)は工業的に重要です。 タングステン鉱物は通常花崗岩に埋め込まれているため、平均タングステン濃度は 1 ~ 2% です。
カザフスタン、中国、カナダ、米国が最大の埋蔵量を持っています。 ボリビア、ポルトガル、ロシア、ウズベキスタン、韓国でも鉱床が知られています。 世界のタングステン生産量は年間 49 ~ 50 千トンで、そのうち 41 トンが中国、3.5 トンがロシアです。 カザフスタン0.7、オーストリア0.5。 タングステンの主な輸出国: 中国、韓国、オーストリア。 主な輸入者:米国、日本、ドイツ、英国。
アルメニアやその他の国にもタングステン鉱床があります。
応用
 タングステンの耐火性と延性により、照明器具の白熱フィラメントや受像管、その他の真空管にはタングステンが不可欠です。
タングステンの耐火性と延性により、照明器具の白熱フィラメントや受像管、その他の真空管にはタングステンが不可欠です。
タングステンはその高密度のため、カウンターウェイト、サブ口径および後退フィン砲弾の装甲貫通コア、装甲貫通弾丸コア、および飛行を安定させる高速ジャイロスコープ ローターに使用される重合金の基礎となります。弾道ミサイル(最大18万rpm)。
タングステンはアルゴンアーク溶接の電極として使用されます。 タングステンを含む合金は、耐熱性、耐酸性、硬度、耐摩耗性が特徴です。 手術器具(アマロイ合金)、戦車の装甲、魚雷の砲弾や砲弾、航空機やエンジンの最も重要な部品、放射性物質を保管する容器などの製造に使用されています。 タングステンは、最高グレードの工具鋼の重要な成分です。 タングステンは、高温真空抵抗炉で発熱体として使用されます。 タングステンとレニウムの合金は、熱電対などの炉で使用されます。
機械工学における金属および非金属構造材料の機械加工 (旋削、フライス加工、平削り、彫刻)、坑井掘削、および鉱業では、超硬合金および炭化タングステンをベースとした複合材料が広く使用されています (例: pobeditコバルトマトリックス中の WC 結晶で構成され、ロシアで広く使用されているグレード - VK2、VK4、VK6、VK8、VK15、VK25、T5K10、T15K6、T30K4)、および炭化タングステン、炭化チタン、炭化タンタルの混合物 (TT)耐熱鋼のハツリ鍛造品やカンナ鍛造品、高強度材料のロータリーハンマードリルなど、特に困難な加工条件に適したグレードです。 鋼および鉄ベースの合金の合金元素(多くの場合モリブデンと一緒に)として広く使用されています。 「高速度」に分類され、文字 P で始まるマークが付いている高合金鋼には、ほとんどの場合タングステンが含まれています。 (P18、P6M5。急速 - 高速、速度から)。
硫化タングステン WS 2 は高温 (500 °C まで) 潤滑剤として使用されます。 一部のタングステン化合物は触媒や顔料として使用されます。 タングステン酸塩単結晶 (タングステン酸鉛、カドミウム、タングステン酸カルシウム) は、核物理学および核医学において X 線およびその他の電離放射線のシンチレーション検出器として使用されます。
ジテルル化タングステン WTe 2 は、熱エネルギーを電気エネルギー (熱起電力約 57 μV/K) に変換するために使用されます。 人工放射性核種 185 W は、物質研究における放射性トレーサーとして使用されます。 安定した 184 W は、熱中性子捕獲断面積が小さい (約 2 バーン) 唯一の一般的なタングステン同位体であるため、固相核ロケット エンジンに使用されるウラン 235 との合金の成分として使用されます。
タングステン - W
分類
| ニッケル・ストルンツ (第 10 版) | 1.AE.05 |
| ダーナ (第7版) | 1.1.38.1 |
導入
科学技術における希少元素の重要性は年々高まっており、希少元素と非希少元素の境界はますます曖昧になってきています。 現代の分析化学者は、タングステン、モリブデン、バナジウム、チタン、ジルコニウム、その他の希少元素の測定に取り組むことがますます増えています。
すべての元素の混合物を分析することは非常にまれなケースです。
鉱物に含まれる希少元素と非希少元素の多くの組み合わせは非常に複雑であるため、分析には希少元素化学に関する広範な経験と知識が必要です。
元素をグループに分離したり、任意の 1 つの元素を分離するには、沈殿反応だけでなく、有機溶媒による化合物の抽出、揮発性化合物の蒸留、電気分解などの他の方法も使用されます。
一部の希少元素は化学的方法で分離して測定することが難しいため、これらの測定は物理的方法 (スペクトル、発光など) によって行われます。
非常に少量の微量元素が検出された場合は、特別に選択された別の元素である「キャリア」との元素の共沈に基づいて化学濃縮法が使用されます。 担体要素は、分析のさらなる過程を妨げないような方法で選択されます。
最も重要な希少元素の 1 つはタングステンです。 この論文では、タングステンの定性的検出に関連するいくつかの問題を検討したいと思います。
タングステンの発見の歴史
「タングステン」という言葉は、この金属が発見されるずっと前から存在していました。 ドイツの医師で冶金学者のゲオルギウス・アグリコラ (1494-1555) でさえ、一部の金属をタングステンと呼んでいました。 「タングステン」という言葉にはさまざまな意味がありました。 特に、それは「オオカミの唾液」と「オオカミの泡」の両方を意味しました。 怒ったオオカミの口から出る泡。 14 世紀から 16 世紀の冶金学者は、錫を製錬するときに、いくつかの鉱物の混合により金属が大幅に失われ、金属が「泡」、つまりスラグに変わることに気づきました。 有害な不純物は鉄マンガン石(Mn、Fe)WO4 という鉱物で、見た目はスズ鉱石 - 錫石(SnO2)に似ていました。 中世の冶金学者は鉄マンガン石を「タングステン」と呼び、「狼が羊のように錫を盗んで食い荒らす」と述べた。
タングステンは、1783 年にスペインの化学者デ・エルハル兄弟によって初めて入手されました。 さらに前の1781年。 - スウェーデンの化学者シェーレは、CaWO4 という組成の鉱物から三酸化タングステン WO3 を単離しました。この鉱物は後に「シーライト」として知られるようになりました。 したがって、タングステンは長い間シーリウムと呼ばれていました。
イギリス、フランス、アメリカではタングステンの呼び方が異なります。タングステンはスウェーデン語で「重い石」を意味します。 19世紀のロシアでは、タングステンは「アザミ」と呼ばれていました。
化学元素の周期表における位置
タングステンは化学元素の周期系の VI 族の元素であり、シリアル番号は 74、原子量は 183.85 です。
天然タングステンは、安定同位体と質量の混合物で構成されています。
タングステンについては、質量 174 ~ 188 の放射性同位体も知られています。
タングステンの物理化学的性質とその応用
タングステン化学定性検出
純金属タングステンは銀白色の金属で、外観は鋼に似ており、体心立方晶格子を持っています。 粉末状 - ダークグレー色。
タングステンの物理定数:
融点。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 3380~3430℃
沸点。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 .5900℃
密度 (20 ℃) 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 .19.3 g/cm3
比熱容量(20℃にて)。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 .0.032 cal/g* oC
融解熱。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 0.44カロリー/g
気化熱。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 .. . 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 。 .1.83 カロリー/g
タングステンの蒸気圧を表 1 に示します (付録を参照)。
タングステンは、金属の中で最も高い融点と最も低い蒸気圧を持っています。 タングステン ワイヤは、最高の引張強度と最大 420 kg/mm2 の降伏強度を備えています。
今日、タングステンは科学技術の分野で広く使用されています。 これは、鋼の合金化、超硬合金の基礎、航空およびロケット技術用の耐熱合金の成分、電気真空装置の陰極および白熱灯のフィラメントの製造に使用されます。 タングステン合金は高い耐熱性(1650℃での極限強度は175~253 MPa)を持っていますが、脆く、600℃を超えると空気中で激しく酸化します(保護コーティングなしでは、真空および還元性または中性環境でのみ使用できます)。雰囲気)。 電離放射線をよく吸収します。 これらは、発熱体、熱シールド、放射性薬剤を保管するための容器、熱エミッター、最大 2500℃ の温度を測定するために使用される熱電対電極 (レニウムを含む合金) の製造に使用されます。
化学的性質
タングステンは最も耐食性の高い金属の 1 つです。 常温では水や空気に対して耐性がありますが、400~500℃の温度では著しく酸化し、高温では激しく酸化して黄色の三酸化タングステンを形成します。 非常に高温でも水素と相互作用せず、2000℃以上の温度では窒素と相互作用して窒化物 WN2 を形成します。 固体炭素は 1100 ~ 1200 ℃でタングステンと反応し、炭化物 WC および W2C を形成します。 低温では、硫酸、塩酸、硝酸、フッ化水素酸、王水はタングステンに影響を与えません。 100℃の温度では、タングステンはフッ化水素酸とは相互作用せず、塩酸や硫酸とは弱く相互作用し、硝酸や王水とはより速く反応します。 フッ化水素酸と硝酸の混合液に素早く溶解します。 低温のアルカリ溶液はタングステンには影響を与えません。 溶融アルカリは、空気の存在下、または酸化剤 (硝酸塩、塩素酸塩、二酸化鉛など) の存在下でタングステンを集中的に溶解し、塩を形成します。
タングステン原子内の電子の分布は、1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 5d4 6s2 です。 タングステンのイオン化ポテンシャル: I1=7.98eV; I2=17.7eV。 原子半径rme=1.40Ao。
イオン半径:
化合物では、タングステンは +2、+3、+4、+5、+6 の酸化状態を示します。 より高い酸化状態では、タングステンは酸性の特性を持ち、より低い酸化状態では塩基性の特性を持ちます。 酸化状態が +2、+3 の化合物は不安定です。 二価タングステンはハロゲン化物の形でのみ知られています。 安定な複合シアン化物は、固体のタングステン(IV)化合物から単離されています。 タングステン(V)および(VI)化合物は、分析において実用上最も重要です。
溶液中でのタングステンの挙動は、単純な化合物が存在しないため、特に酸性溶液中では複雑です。 タングステンの分析化学において非常に重要なのは、錯体を形成する傾向が大きいことです。 複雑な化合物では、個々の元素の個々の特性が単純な化合物よりも明確に現れるため、タングステンの錯化は、同様の特性を持つ元素の存在下での測定に広く使用されています。
タングステン(II)および(III)化合物は強力な還元剤ですが、タングステン(V)化合物の酸化力は弱いです。
タングステンとその化合物の熱力学データを表 2 に示します (付録を参照)。
20 世紀の 40 年代までは、タングステンの分析化学はモリブデンの分析化学とともに発展し、前者は重量分析による測定方法が特徴でした。 近年、タングステン配位化合物の化学研究が成功裏に行われており、その一部は分析化学において物理的および物理化学的方法によるタングステンの定量に使用され、成功しています。
タングステンとモリブデンの特性の類似性は、互いの存在下での分離と測定の困難さを説明しています。 ただし、価電子の分布の違いと、タングステンの電子殻が経験するランタニドの収縮現象により、これらの元素の化学的性質の一部に違いが生じます。 たとえば、タングステン (VI) の水溶液は鉱酸の存在下で重合および加水分解する傾向がモリブデン (VI) の水溶液よりも強いです。 タングステンは、特定の低酸化状態に戻すのがより難しく、モリブデンとは異なり、その安定化は複雑で、常に成功するとは限りません。
高品質のタングステン検出
タングステンの化学は非常に複雑です。 この元素はさまざまな酸化度を持ち、多数の化合物を形成します。 ここでは、合金が酸に溶解したときに形成されるタングステン化合物の特性のみを考慮します。 これらの合金を溶解するには、2Nと混合した濃硝酸が使用されます。 硫酸または王水では、タングステンは最も高い酸化状態 +6 になります。 したがって、タングステン(VI)化合物の特性に焦点を当てます。
WO42- イオンの部分反応:
1. 酸。 タングステン酸塩の溶液が塩酸などの濃鉱酸にさらされると、タングステン酸の白い沈殿物が沈殿します。
WO42-+2H++H2O = WO3*2 H2O。
WO3*2H2Oは沸騰すると黄色のWO3*H2Oに変わります。 タングステン酸は濃酸に不溶です (MoO3*H2O とは異なります)。 その形成反応は、WO42- を他のイオンから分離するために使用されます。
2. 酸性溶液中の硫化水素 H2S は WO42- を沈殿させません。
3. 硫化アンモニウム (NH4)2S は、タングステン酸塩と水溶性チオ塩を形成します。例:
WO42- + 8NH4+ +4S2-+ 4H2O = WS42- + 8NH4OH。
酸性化すると、チオサールは分解して薄茶色の沈殿物 WS3 を形成します。
4. WO42-の回収。 塩酸または硫酸で酸性化したタングステン酸塩溶液を金属亜鉛で処理します。 最初に形成されたタングステン酸の沈殿は、タングステン(VI) および (V) 化合物を含むさまざまな組成の生成物の形成により青色に変わります。
Zn + 2WO42-+6H+ = W2O5+Zn2++3H2O。
同じ化合物は、亜鉛を塩化スズ(II)の溶液に置き換えることによって得られます。
硫化水素分析法では、タングステンはヒ素のサブグループとして分類されます。 しかし、酸性環境における硫化水素の作用下では硫化物を形成せず、アルカリ性環境におけるアンモニウムおよびアルカリ金属硫化物または硫化水素の作用下でのみ硫化物を形成する。 過剰な硫化物に溶解してチオ塩を形成します。
Na2WO4 + 4 (NH4)2S + 4 H2O = Na2WS4 + 8 NH4OH。
チオ塩の溶液が酸性化すると、薄茶色の硫化タングステンが沈殿します。
Na2WS4 + 2 HCl = 2 NaCl + H2S + WS3、
過剰な塩酸に溶けます。 しかし、WO42- イオンは塩酸の作用下で銀基 (Ag+、Hg22+、Tl(I)、Pb2+) とともに難溶性のタングステン酸の形で沈殿するため、ほとんどのカチオンから分離されます。
硫酸水素を含まない分析スキームでは、タングステンは塩酸の作用によりタングステン酸の形で分離されることも提案されています。 それと一緒に、Ag+、Hg22+、Tl(I)、Pb2+ のイオンが塩化物の形で沈殿します。 タングステン存在下でのカチオン分析の系統的な進行状況を表 3 に示します (付録を参照)。
タングステンの定性分析はあまり開発されていません。 タングステン酸塩に対する鉱酸の作用による難溶性タングステン酸の沈殿が主に使用されます。 これらの条件下では、タングステン酸とともにケイ酸が沈殿します。 タングステンは、沈殿物をアンモニアで処理することによって後者から分離され、その後、濾液中に見出されます。 無機試薬では、チオシアン酸アルカリ金属およびアンモニウムがチタン(III)およびスズ(II)還元剤の存在下で最もよく使用され、有機試薬ではトルエン-3,4-ジチオールが使用されます。 タングステンの測光測定に推奨されている試薬を検出に使用できる可能性があります。これらの試薬は感度が高く、特に酸加水分解などによるタングステンの分離後は非常に信頼性が高くなります。 タングステンの重量測定に推奨される試薬は、タングステンとともに特徴のない堆積物を形成するため、タングステンの検出にはほとんど役に立ちません。
コレンマンは、塩化アンモニウムを使用してタングステンを検出することを提案しました。タングステン酸アンモニウムの無色の結晶はダイヤモンドや棒のような形をしています。 感度 1 滴のタングステン 0.15 µg、最大希釈 1:4 * 104。 検出は、塩化物、硫酸塩、100 倍量のモリブデン酸塩、30 倍量のバナジン酸塩によって妨げられません。
ロダン法では、鉱石中の 0.05 ~ 1% の三酸化タングステン WO3 と岩石中の 10 ~ 4% のタングステンを滴下法で検出することができます。
鉱石中のタングステンの滴下検出。 0.05 ~ 1% の三酸化タングステンの検出は、10% のモリブデンおよびバナジウムによって妨げられません。 5% クロム; ヒ素とアンチモンはそれぞれ 2% ずつ含まれていますが、バナジウムとクロムを分離することをお勧めします。
粉砕したサンプルを約5mgと融合? 20mgの水酸化ナトリウム、約3mgの過酸化ナトリウムを溶融物に添加し、再度溶融する。 溶融物の黄色はクロムの存在を示します。 数滴の水を溶融物に加え、加熱し、磁器るつぼに移し、塩酸で酸性化します。 溶液を水浴中でほぼ乾燥するまで蒸発させ、残留物を塩酸で湿らせ、水で希釈し、濾過する。 濾過ケーキを熱アンモニア溶液(1:1)で処理し、熱水で洗浄し、濾液と洗浄水を合わせ、試薬溶液を1滴添加する(水100ml中にチオシアン酸カリウム30g)。少量まで蒸発させ、濃塩酸 1 ~ 2 滴を加え、酸、塩化スズ(II) の 10% 溶液を 1 滴、および塩化チタン(III) の 0.5% 塩酸溶液を 1 滴加えます。 :1)。 タングステンが存在すると黄色が現れます。
鉱石や岩石中のタングステンの検出。 検出?1 タングステンの 10 ~ 4% は、モリブデン、セレン、テルル、大量の鉄、バナジウム、クロム、二酸化ケイ素によって妨害されます。 硫化物サンプルは焼成され、焼成後にさらに粉砕されます。
細かく粉砕した物質 0.5 g を試験管またはマイクログラス中で、水浴中で加熱しながら 2 ml の塩酸で 30 分間処理します。 ヒ素が存在する場合、臭化カリウムの存在下でヒドラジンの作用によりヒ素が除去され、試薬を元の体積の半分まで導入した後、液体が蒸発します。 残渣を2倍量の水に溶解し、溶液を綿棒で濾過し、1~2mlの水で洗浄する。 濾液と洗浄水を蒸発乾固し、1~2滴の水に溶解し、水酸化鉄が完全に沈殿するまで25%水酸化カリウム溶液を滴下し、飽和チオシアン酸アンモニウム溶液を3滴加え、混合する。 、塩化スズ(II)の40%溶液を赤色が消えるまで加えます。 タングステンが存在すると、黄緑色が現れます。
タングステンの検出感度を0.01μgまで高めるには、アニオン樹脂粒子上で反応を行うことをお勧めします。 検出は、100 ~ 1000 μg の La、Ce(IV)、Zr、Th、Mn、Fe、Ni、Zn、Cd、Al、Ga、In、Ge、Sn (IV)、Pb、Sb (III) によって妨げられません。 )、Bi、F-、Br-、I-、NO3-、SO32-、SO42-、HPO42-、B4O72-、HCOO-、C2O42-、クエン酸塩および酒石酸塩。 Pd、Pt、Ag、Au、Hg、As、Se、Te が干渉します。
モリブデンの存在下、溶液を硫酸で1〜2Mの濃度まで酸性化し、モリブデンを等量のアセチルアセトンとクロロホルムの混合物で2回抽出し、水層を濾過し、蒸発させて少量の硝酸にする。有機物を破壊するために水酸化ナトリウムを導入し、水酸化ナトリウムを0.01Mの濃度で添加します。 溶液を白いタイル板の上に置き、Dauex-1-x-1 または 1-x-2 陰イオン交換樹脂を数粒加え、数分後に 10% 塩化スズ(II) 溶液を 1 滴加えます。濃塩酸と3%チオシアン酸アンモニウム溶液を加える。 タングステンが存在すると、粒子は緑色に変わります。 蛍光灯の下で顕微鏡で粒子を観察することをお勧めします。
鋼中のタングステンの滴下検出。 Kullberg は、タングステン酸に対する過酸化水素の作用によって形成されるペルオキソタングステン酸が、ベンジジンの酢酸溶液をオレンジ、赤、茶色に着色する能力に基づいた反応を提案しています。 得られる化合物は過酸化水素に対して耐性があります。
酸混合物 (30% 硫酸 1 部と濃硝酸 1 部) を 1 滴、洗浄した鋼表面に置きます。 2~3分後、大過剰の過酸化ナトリウムを加えて混合し、沸騰が止まるまで10%アンモニア溶液を一滴ずつ加えます。 沈殿物の一部をろ紙で捕集し、その上に新たに調製したベンジジンの 1% 氷酢酸溶液を 2 ~ 3 滴滴下します。 タングステンが存在すると、オレンジ、赤、茶色が現れます。
鋼では、タングステンはジチオールによって検出できます。 モリブデン、ジルコニウム、銅、その他の鋼成分は干渉しません。
0.5 ~ 0.6 g の鋼サンプルを 10 ml の 6 M 塩酸に溶解します。 溶液の一部を塩化スズ(II)とともに加熱してモリブデン(VI)をモリブデン(III)に還元し、ジチオールのメタノール溶液を添加する。 タングステンが存在すると、青緑色が現れます。
ローダミン C を使用した場合、タングステンの検出感度は 1 滴の溶液中で 0.001 ~ 0.0005 mg です。 タングステン酸 H2WO4 を単離し、水酸化ナトリウムに溶解して、弱酸性環境でタングステンを検出することをお勧めします。 タングステンを分離しない場合の検出は、I-、Br-、SCN-、Cr2O72-、S2O82-、MnO4-、ClO4-、S2O32- アニオンを含む多くのイオンによって妨げられます。
ペーパークロマトグラムでのタングステンの検出にはローダミン C が推奨されます。 これを行うために、1M 硫酸中のローダミン C の 0.025% 溶液と臭化カリウムの 20% 溶液をスプレーします。 タングステンの存在は、スポットの色または発光によって識別できます。
陰極または紫外線にさらされると、灰重石は青色光で強く発光します。
タングステンの性質
タングステン- それは金属です。 海水にも空気中にも存在せず、地殻中にはわずか 0.0055% しか存在しません。 そのようにして タングステン、元素、で74位に立っています。 フランスの首都で開催された万国博覧会によって、産業向けに「公開」されました。 それは1900年に起こりました。 展示の目玉となったのは タングステン鋼.
この組成物は非常に硬かったので、どんな材料でも切断することができました。 数千度の温度でも「無敵」を保ったため、耐赤化性と呼ばれました。 展示会を訪れた各国のメーカーが開発を採用した。 合金鋼の生産は世界規模になりました。
興味深いことに、この元素自体は 18 世紀に発見されました。 1781 年、スウェーデンのシェーラーはタングステンという鉱物を使った実験を行いました。 化学者はそれを硝酸に入れることにしました。 科学者は分解生成物の中に、銀色がかった未知の灰色の金属を発見しました。 実験が行われた鉱物は後に灰重石と改名され、新元素は タングステンと呼ばれる.
しかし、その特性を研究するのに多くの時間がかかったので、この金属の価値ある用途が発見されたのはずっと後になってからでした。 名前はすぐに決まりました。 タングステンという言葉以前から存在していました。 スペイン人はこれを国の鉱床で見つかる鉱物の一つと呼びました。
実際、石の組成には元素番号 74 が含まれていました。 外側では、金属は発泡したかのように多孔質です。 したがって、別の例え話が役に立ちました。 ドイツ語でタングステンは文字通り「オオカミの泡」を意味します。

この金属の融点は、最も耐熱性の高い元素である水素の融点に匹敵します。 したがって、インストールします タングステン軟化指数彼らは百年間それができなかった。 数千度まで加熱できる炉はありませんでした。
シルバーグレーの元素の「利点」が「見抜かれた」とき、彼らはそれを工業規模で採掘し始めました。 1900 年の展示会では、硝酸を使用した昔ながらの方法で金属が抽出されました。 しかし、タングステンは今でもこの方法で採掘されています。
タングステン採掘
ほとんどの場合、三酸化物物質はまず鉱石廃棄物から得られます。 700度で処理され、純粋な金属が粉塵の形で得られます。 粒子を柔らかくするには水素に頼らなければなりません。 その中で タングステンが溶けてる摂氏3000度で。
カッター、パイプカッター、フライスなどに使用される合金です。 金属加工用 タングステンを使用部品製造の精度を高めます。 金属表面に接触すると摩擦が高くなり、作業面が非常に熱くなります。 エレメント番号 74 のない切断機や研磨機は、それ自体が溶ける可能性があります。 これにより、カットが不正確で不完全になります。
タングステンは溶解が難しいだけでなく、加工も困難です。 硬度スケールでは、金属は 9 番目の位置を占めます。 コランダムには同じ数の点があり、その破片は、たとえばサンドペーパーを作るのに使用されます。 ダイヤモンドだけが硬いです。 したがって、タングステンはその助けを借りて加工されます。
タングステンの用途
74番目の要素の「堅実さ」が魅力的です。 灰色がかったシルバーの金属との合金で作られた製品は、もちろん表面や同じダイヤモンドで傷をつけない限り、傷がついたり、曲がったり、壊れたりすることはありません。

タングステンジュエリーにはもう一つの紛れもない利点があります。 金、銀、プラチナ、さらにはそれらとの合金とは異なり、アレルギー反応を引き起こしません。 宝飾品には、炭化タングステン、つまり炭素との化合物が使用されます。
人類史上最も硬い合金として認められています。 磨かれた表面は光を完璧に反射します。 宝石商はそれを「グレーミラー」と呼んでいます。
ちなみに宝石は マスターはタングステンに注目しました 20世紀半ばに弾丸の核、砲弾、防弾チョッキ用のプレートがこの物質から作られるようになった。
高級シルバー宝飾品の壊れやすさに関する顧客の苦情により、宝石商は新しい要素を思い出し、それを自分たちの業界に適用しようとすることを余儀なくされました。 さらに、価格も変動し始めました。 タングステンは、もはや投資対象として認識されていないイエローメタルの代替品となっています。
貴金属であるため、 タングステンのコストたくさんのお金。 卸売市場ではキログラム当たり少なくとも50ドルを要求する。 世界の産業界は年間 30,000 トンの元素 No. 74 を費やしています。 90%以上が冶金産業に吸収されます。

のみ タングステン製核廃棄物を保管するための容器。 金属は破壊的な光線を透過しません。 希少元素を合金に添加して手術器具を製造します。
冶金目的で使用されないものは化学産業に引き取られます。 たとえば、リンを含むタングステン化合物はワニスや塗料の基礎となります。 日光によって崩れたり色あせたりすることはありません。
あ タングステン酸ナトリウム溶液湿気や火に強い。 ダイバーや消防士のスーツに使用される防水・防火生地にどのような素材が含浸されているのかが明らかになりました。
タングステン鉱床
ロシアにはいくつかのタングステン鉱床があります。 彼らはアルタイ、極東、北コーカサス、チュクチ、ブリヤートに位置しています。 国外では、この金属はオーストラリア、米国、ボリビア、ポルトガル、韓国、中国で採掘されています。
中王国には、ブリキ石を探しに中国に来た若い探検家についての伝説さえあります。 その学生は北京の家の一軒に定住した。

無駄な捜索の後、その男はオーナーの娘の話を聞くのが大好きでした。 ある晩、彼女は家庭用ストーブを作った黒い石の話をしました。 ブロックは崖から建物の裏庭に落ちていたことが判明した。 つまり、学生はそれを見つけられませんでしたが、タングステンを見つけたのです。
周期表の原子番号 74 で、記号 W (ラテン語: Wolframium) で示される、固体の灰色の遷移金属です。 主な用途は、冶金学における耐火材料の基礎としてです。 非常に耐火性が高く、標準条件下では耐薬品性があります。
歴史と名前の由来
ウルフラミウムという名前は、16 世紀に知られていた鉱物のウルフラマイトからこの元素に移されました。 「狼の泡」、ラテン語で「Spuma lupi」、ドイツ語で「Wolf Rahm」と呼ばれます。 この名前は、錫鉱石に含まれるタングステンが錫の精錬を妨げ、錫をスラグの泡に変えたという事実によるものです(「狼が羊を貪るように錫を貪る」)。
現在、米国、英国、フランスでは、タングステンを「タングステン」(スウェーデン語:tung sten - 「重い石」)という名前が使用されています。
1781年、有名なスウェーデンの化学者シェーレは、鉱物灰重石を硝酸で処理して、黄色の「重い石」を得ました。 1783年、スペインの化学者エリュアール兄弟は、サクソン鉱物の鉄マンガン石からアンモニアに可溶な新しい金属の黄色の酸化物を得たと報告した。 さらに、兄弟の一人、ファウストは 1781 年にスウェーデンにいて、シェーレと連絡を取り合いました。 シェーレはタングステンの発見を主張しなかったし、エリュアール兄弟も自分たちの優先順位を主張しなかった。
レシート
タングステンを得るプロセスは、鉱石精鉱から三酸化物WO 3 を分離し、その後、約100℃の温度で水素を用いて金属粉末に還元するというサブステージを経ます。 700℃。 タングステンの融点は高いため、緻密な形状を得るには粉末冶金法が使用されます。得られた粉末をプレスし、水素雰囲気中で 1200 ~ 1300 °C の温度で焼結し、電流を流します。 金属は 3000 °C に加熱され、焼結が起こりモノリシック材料になります。 その後の精製と単結晶形態の取得には、ゾーンメルティングが使用されます。
プロパティ
物理的な
タングステンは明るい灰色の金属で、融点と沸点が最も高いことが証明されています(シーボーギウムはさらに耐火性が高いと考えられていますが、これまでのところ断言できません。シーボーギウムの寿命は非常に短いです)。
タングステンは、最も重く、最も硬く、最も高融点の金属の 1 つです。 純粋な形では、プラチナに似た銀白色の金属で、約 1600 °C の温度で容易に鍛造でき、細い糸に引き抜くことができます。
化学薬品
価数は2から6まであり、最も安定しているのは6価のタングステンです。 3 価および 2 価のタングステン化合物は不安定であり、実用的な意味はありません。
タングステンは高い耐食性を持っています。室温では空気中で変化しません。 赤熱温度ではゆっくりと酸化してVI酸化タングステンになります。 塩酸、硫酸、フッ化水素酸にはほとんど溶けません。 硝酸や王水では表面から酸化します。 硝酸とフッ化水素酸の混合物に溶解し、タングステン酸を形成します。 タングステン化合物の中で最も重要なものは、三酸化タングステンまたは無水タングステン、タングステン酸塩、一般式 Me 2 WO x の過酸化物化合物、およびハロゲン、硫黄、炭素を含む化合物です。 タングステン酸塩は、他の遷移金属を含むヘテロポリ化合物などのポリマーアニオンを形成しやすいです。