“Tıpkı bir sanatçı veya şair gibi bir matematikçi de modeller yaratır. Ve eğer kalıpları daha istikrarlıysa, bu sadece fikirlerden oluştuğu içindir... Bir matematikçinin desenleri, tıpkı bir sanatçının veya şairin desenleri gibi, güzel olmalı; Renkler veya kelimeler gibi fikirlerin de birbiriyle uyumlu olması gerekir. Güzellik ilk şart: Dünyada çirkin matematiğe yer yok».
G.H.Hardy
İlk bölümde oldukça ilkellerin var olduğuna dikkat çekildi. basit işlevler artık aracılığıyla ifade edilemeyen temel işlevler. Bu bağlamda, antitürevlerinin temel fonksiyonlar olduğunu doğru bir şekilde söyleyebileceğimiz fonksiyon sınıfları çok büyük pratik önem kazanır. Bu fonksiyon sınıfı şunları içerir: rasyonel fonksiyonlar, iki oranını temsil eden cebirsel polinomlar. Birçok problem rasyonel kesirlerin entegrasyonuna yol açmaktadır. Bu nedenle bu tür fonksiyonları entegre edebilmek çok önemlidir.
2.1.1. Kesirli rasyonel fonksiyonlar
Rasyonel kesir(veya kesirli rasyonel fonksiyon) iki cebirsel polinomun ilişkisi olarak adlandırılır:
nerede ve polinomlardır.
şunu hatırlatalım polinom (polinom, tüm rasyonel fonksiyon ) Nderece formun bir fonksiyonu denir
Nerede ![]() – gerçek sayılar. Örneğin,
– gerçek sayılar. Örneğin,
![]()
– birinci dereceden polinom;
– dördüncü dereceden polinom vb.
Rasyonel kesir (2.1.1) denir doğru, eğer derece, dereceden düşükse, yani. N<M aksi takdirde kesir denir yanlış.
Herhangi bir uygunsuz kesir, bir polinomun (tam sayı kısmı) ve uygun kesirin (kesirli kısım) toplamı olarak temsil edilebilir. Uygunsuz bir kesirin tam ve kesirli kısımlarının ayrılması, polinomları bir "köşe" ile bölme kuralına göre yapılabilir.
Örnek 2.1.1. Aşağıdaki uygunsuz rasyonel kesirlerin tam ve kesirli kısımlarını tanımlayın:
A)  , B)
, B)  .
.
Çözüm . a) “Köşe” bölme algoritmasını kullanarak şunu elde ederiz:

Böylece elde ederiz
 .
.
b) Burada ayrıca “köşe” bölme algoritmasını kullanıyoruz:

Sonuç olarak şunu elde ederiz:
 .
.
Özetleyelim. Genel durumda, rasyonel bir kesirin belirsiz integrali, polinomun ve uygun rasyonel kesrin integrallerinin toplamı olarak temsil edilebilir. Polinomların ters türevlerini bulmak zor değildir. Bu nedenle, aşağıda esas olarak uygun rasyonel kesirleri ele alacağız.
2.1.2. En basit rasyonel kesirler ve bunların entegrasyonu
Uygun rasyonel kesirler arasında dört tür vardır ve bunlar şöyle sınıflandırılır: en basit (temel) rasyonel kesirler:
|
3) |
4) |
bir tam sayı nerede, ![]() , yani ikinci dereceden üç terimli
, yani ikinci dereceden üç terimli ![]() gerçek kökleri yoktur.
gerçek kökleri yoktur.
Tip 1 ve tip 2'nin basit kesirlerini entegre etmek çok fazla zorluk yaratmaz:
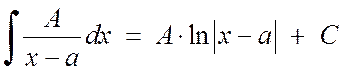 , (2.1.3)
, (2.1.3)
 . (2.1.4)
. (2.1.4)
Şimdi 3. türdeki basit kesirlerin integralini ele alalım, ancak 4. türdeki kesirleri dikkate almayacağız.
Formun integralleriyle başlayalım
 .
.
Bu integral genellikle paydanın tam karesinin ayrılmasıyla hesaplanır. Sonuç, aşağıdaki formun bir tablo integralidir
 veya
veya  .
.
Örnek 2.1.2.İntegralleri bulun:
A)  , B)
, B) 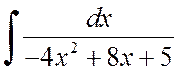 .
.
Çözüm . a) İkinci dereceden bir üç terimliden tam bir kare seçin:
Buradan buluyoruz
b) İkinci dereceden bir üç terimliden tam bir kareyi izole ederek şunu elde ederiz:
Böylece,
 .
.
İntegrali bulmak için
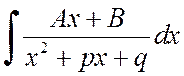
paydanın türevini payda izole edebilir ve integrali iki integralin toplamına genişletebilirsiniz: bunlardan ilki ikame yoluyla ![]() görünüşe geliyor
görünüşe geliyor
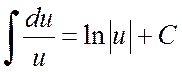 ,
,
ve ikincisi - yukarıda tartışılana.
Örnek 2.1.3.İntegralleri bulun:
 .
.
Çözüm
. Dikkat 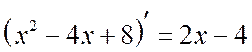 . Paydanın türevini payda izole edelim:
. Paydanın türevini payda izole edelim:
İlk integral ikame kullanılarak hesaplanır ![]() :
:
İkinci integralde paydadaki tam kareyi seçiyoruz
Sonunda elde ettik
2.1.3. Uygun rasyonel kesir açılımı
basit kesirlerin toplamı için
Herhangi bir uygun rasyonel kesir ![]() basit kesirlerin toplamı olarak benzersiz bir şekilde temsil edilebilir. Bunu yapmak için paydanın çarpanlara ayrılması gerekir. Yüksek cebirden, gerçek katsayılı her polinomun
basit kesirlerin toplamı olarak benzersiz bir şekilde temsil edilebilir. Bunu yapmak için paydanın çarpanlara ayrılması gerekir. Yüksek cebirden, gerçek katsayılı her polinomun
Bu kadar küçük bir madde parçacığını doğrudan ölçemeyeceğimiz açıktır. Basit hesaplamalar yoluyla moleküllerin boyutunu belirleyebileceğimiz bir deney yapacağız. Petrol ürünlerinin (yağlama yağları, dizel yakıt vb.) su yüzeyinde oluşturduğu ince renkli filmleri elbette görmüşsünüzdür. İnce filmlerin rengi, filmin üst ve alt yüzeylerinden yansıyan ışık ışınlarının üst üste gelmesi nedeniyle oluşur; bu olaya ışık girişimi adı verilir. Aynı sebepten ötürü sabun köpüğü gökkuşağının tüm renkleriyle parıldar.
Fizik derslerinde girişim olgusunu inceleyeceksiniz. Şimdi filmin kalınlığıyla ilgileniyoruz; ne kadar kalın olduğunu hiç merak ettiniz mi? Filmin kalınlığını belirlemek çok basittir: hacmini yüzey alanına bölmeniz gerekir. Eski denizciler bile, suyun yüzeyine bitkisel yağ dökülürse çok geniş bir noktaya yayılacağını fark ettiler (o zamanlar, fırtına sırasında denizi bu şekilde "sakinleştirebileceğinize" dair oldukça garip bir görüş ortaya çıktı). Muhtemelen su üzerindeki yağ lekesinin alanını ölçen ilk kişi, görüntüsü yüz dolarlık banknotta görünen seçkin Amerikalı bilim adamı ve diplomat Benjamin Franklin (1706-1790) idi. En ünlü icadı paratonerdir (ya da daha doğrusu paratonerdir). 1774'te Franklin, İngiltere ile Amerika Birleşik Devletleri arasındaki başka bir anlaşmazlığı çözmek için Avrupa'ya gitti. Müzakerelerden boş zamanlarında su yüzeyindeki yağlı filmlerle deneyler yaptı. Küçük göletin tüm yüzeyine bir kaşık bitkisel yağın yayılması onu şaşırttı. Suya bitkisel olmayan bir yağ dökerseniz, ancak viskoz olmayan bir makine yağı dökerseniz, leke o kadar büyük olmayacaktır: bir damla, yaklaşık 20 cm çapında bir daire oluşturur. yaklaşık 300 cm3, bir damlanın hacmi yaklaşık 0,03 cm3'tür. Dolayısıyla film kalınlığı 0,03 cm1 / 300 cm3 = 0,0001 cm = 0,001 mm - 1 mikron olur. Milimetrenin binde biri çok küçük bir değerdir; bu büyüklükteki bir parçacığı her mikroskop göremez.
Peki makine yağı moleküllerinin suya tek kat halinde yayılacağının garantisi var mı? Sonuçta, yalnızca bu durumda filmin kalınlığı moleküllerin boyutuna karşılık gelecektir. Böyle bir garantimiz yok ve nedeni şu. Motor yağını oluşturan moleküllere hidrofobik denir (Yunanca "hidrofobik" - "sudan korkar" kelimesinden çevrilmiştir). Birbirlerine oldukça iyi "bağlanırlar", ancak su molekülleri konusunda isteksizdirler. Makine yağına benzer bir madde su yüzeyine dökülürse, üzerinde yüzlerce hatta binlerce moleküler katmandan oluşan oldukça kalın (moleküler standartlara göre) bir film oluşur. Bu tür hesaplamalar başlı başına ilginç olmasının yanı sıra, pratik açıdan da büyük öneme sahiptir. Örneğin, petrolü üretim yerinden binlerce kilometre uzağa taşıyan dev tankerlerin kazalarını önlemek bugüne kadar mümkün değildir. Böyle bir kaza sonucunda denize büyük miktarda petrol dökülebilir ve bu da canlı organizmalar üzerinde zararlı etki yaratabilir. Yağ, motor yağından daha viskoz olduğundan su yüzeyindeki filmi biraz daha kalın olabilir. Böylece kazalardan birinde 500 km3'lük bir alanı kaplayan 120.000 ton petrol döküldü. Basit bir hesaplamanın gösterdiği gibi, böyle bir filmin ortalama kalınlığı 200 mikrondur. Filmin kalınlığı hem petrolün türüne hem de suyun sıcaklığına bağlıdır: Petrolün daha kalın olduğu soğuk denizlerde film daha kalındır, petrolün daha az viskoz hale geldiği sıcak denizlerde ise film daha incedir. Ama her halükarda büyük bir tankerin onbinlerce ton petrolün denize düşmesiyle meydana gelen kaza tam bir felakettir. Sonuçta, eğer dökülen petrolün tamamı ince bir tabaka halinde yayılırsa, çok büyük bir alan oluşacak ve böyle bir filmi ortadan kaldırmak son derece zor olacaktır.
Bir maddenin yalnızca bir molekül katmanı oluşturacak şekilde su üzerine yayılmasını sağlamak mümkün müdür (böyle bir filme monomoleküler denir)? Bunun mümkün olduğu ortaya çıktı, ancak makine yağı veya petrol yerine başka bir madde almanız gerekiyor. Böyle bir maddenin moleküllerinin bir ucunda hidrofilik (yani "suyu seven") atom grubuna, diğer ucunda ise hidrofobik atom grubuna sahip olması gerekir. Bu moleküllerden oluşan bir madde suyun yüzeyine konursa ne olur? Moleküllerin suda çözünmeye çalışan hidrofilik kısmı molekülü suya çekerken, sudan “korkan” hidrofobik kısmı inatla suyla temastan kaçınacaktır. Bu tür karşılıklı "yanlış anlama"nın bir sonucu olarak, moleküller (eğer bir tahta kullanılarak yanlarından hafifçe "bastırılırlarsa"), Şekil 2'de gösterildiği gibi su yüzeyinde sıralanacaklardır. 3.1: Hidrofilik uçları suya girintilidir ve hidrofobik uçları dışarı çıkar.
\6666666666ы/
Pirinç. 3.1. Bu, yüzey aktif madde moleküllerinin su-hava sınırına nasıl yönlendirildiği ve adını 1916'da bu tür katmanların yapısının teorisini yaratan Amerikalı kimyager ve fizikçi Irving Langmuir'den (1881-1957) alan bir "Langmuir barakası" oluşturarak yönlendirilir. sıvıların yüzeyi
Bu şekilde davranan maddelere yüzey aktif maddeler denir. Bunlar arasında örneğin sabun ve diğer deterjanlar; ayçiçek yağının bir parçası olan oleik asit; Palmiye yağı ve balina yağının bir parçası olan palmitik alkol. Bu tür maddelerin su yüzeyine yayılması, makine yağından çok daha ince filmler oluşturur. Bu fenomen uzun zamandır biliniyordu; benzer deneyler 18. yüzyılda da yapıldı. Ancak ancak 19. yüzyılın sonu - 20. yüzyılın başında, İngiliz fizikçi John William Rayleigh (1842-1919), Alman fizikçi Wilhelm Conrad Roentgen (1845-1923) ve çok sayıda bilim insanı tarafından yapılan deneyler sonucunda. diğer bilim adamları, filmin kalınlığının, tek tek moleküllerin boyutlarıyla karşılaştırılabilecek kadar küçük boyutlara ulaşabileceğini gösterdi.
Bu deneylerden birinde İngiliz kimyager Neil Kensington Adam, bildiğimiz maddelerin çoğu molekülü ve iyonunun boyutları 1 nm civarındadır. Böylece, hidrojen moleküllerinin çapı yaklaşık 0,2 nm, iyot - 0,5 nm, etil alkol - 0,4 nm'dir; alüminyum iyonlarının yarıçapı 0,06 nm, sodyum - 0,10 nm, klorür - 0,13 nm, klor - 0,18 nm, iyot - 0,22 nm'dir. Ancak moleküller arasında boyutları moleküler standartlara göre gerçekten astronomik olan devler de var. Böylece, yüksek hayvan ve bitki hücrelerinin çekirdeklerinde kalıtım molekülleri - deoksiribonükleik asitler (DNA) bulunur. Uzunlukları 2.000.000 nm'yi, yani 2 mm'yi aşabilir!
Bu bölümü sonuçlandırmak için, 1908'de Fransız bilim adamı Jean Perrin'in molekülleri "tartmak" için kullandığı ustaca (ama en doğru yöntem değil) yöntem hakkında kısa bir hikaye. Bildiğiniz gibi yükseklik arttıkça hava yoğunluğu azalır. 19. yüzyılın başında Fransız bilim adamı Pierre Laplace, farklı yüksekliklerdeki basıncı hesaplamaya olanak tanıyan bir formül geliştirdi. Bu formüle göre atmosfer basıncı her 6 km'lik yükselişte yarı yarıya düşer. Bu değer elbette yer çekimi kuvvetine ve hava moleküllerinin kütlesine bağlıdır. Hava nitrojen ve oksijenden değil, çok hafif hidrojen moleküllerinden oluşsaydı (oksijen moleküllerinden 16 kat daha hafiftir), o zaman 6 km değil, yaklaşık 16 kat yükseklikte atmosferik basınçta yarı yarıya bir düşüş gözlemlenirdi. daha fazla, yani yaklaşık 100 km. Tersine, eğer moleküller çok ağır olsaydı, atmosfer Dünya yüzeyine “baskılanırdı” ve basınç yükseklikle birlikte hızla düşerdi.
Bu şekilde mantık yürütüyorum. Perrin, moleküller yerine suda asılı duran minik sakız boyası toplarını kullanmaya karar verdi. Aynı boyuttaki toplarla (yaklaşık 1 mikron çapında) bir süspansiyon (emülsiyon) hazırlamaya çalıştı. Daha sonra mikroskobun altına bir damla emülsiyon yerleştirdi ve mikroskop vidasını dikey olarak hareket ettirerek farklı yüksekliklerdeki sakız toplarının sayısını saydı. Laplace formülünün emülsiyonlara oldukça uygulanabilir olduğu ortaya çıktı: Her 6 µm'lik artışta görüş alanındaki topların sayısı yarı yarıya azaldı. 6 km, 6 mikrondan tam olarak bir milyar kat daha büyük olduğundan Perrin, oksijen ve nitrojen moleküllerinin sakız toplarından aynı sayıda kat daha hafif olduğu sonucuna vardı (ve kütleleri zaten deneysel olarak belirlenebilir).
Ve elek prensibine dayalı modern filtrasyon yöntemlerinin genel hatlarıyla incelendiği bir alt bölüm. Ve membranlı arıtma cihazlarının, bu membranlı eleklerdeki gözenek adı verilen “hücrelerin” boyutlarına bağlı olarak suyu farklı niteliklerde arıttığını ima ettiler. Sırasıyla, suyun mikrofiltrasyonu- Bu, dikkate alacağımız membranlı su arıtma sistemlerinin ilk teknolojisidir.
Su mikrofiltrasyonu, asbest parçacıkları, boya, kömür tozu, protozoa kistleri, bakteri, pas gibi büyük moleküller (makromoleküller) seviyesinde suyun arıtılmasıdır. Makrofiltrasyon (suyun) kumu, büyük silt parçacıklarını, büyük pas parçacıklarını vb. etkiler.
Kabaca makrofiltrasyonun elediği partikül boyutlarının (özel bir mikronluk kartuş kullanılması durumunda) 1 mikrometreden büyük partiküller olduğunu söyleyebiliriz. Mikrofiltrasyonun uzaklaştırdığı parçacık boyutu 1 mikrondan 0,1 mikrona kadar parçacıklar.
Şöyle sorabilirsiniz, "Fakat 0,1 mikrona kadar olan parçacıklar çıkarılırsa, mikrofiltrasyonla 100 mikronluk parçacık yakalanmaz mı? Neden '1 mikrondan 0,1 mikrona' yazılıyor, bu bir çelişki?"
Aslında özel bir çelişki yok. Gerçekten de suyun mikrofiltrasyonu hem bakterileri hem de büyük kum parçalarını ortadan kaldıracaktır. Ancak mikrofiltrasyonun amacı büyük kum parçalarını çıkarmak değildir. Mikrofiltrasyonun amacı "belirli bir boyut aralığındaki parçacıkları uzaklaştırmaktır." O zaman nasıl olurdu O Daha büyük parçacıklar arıtıcıyı tıkayacak ve ek maliyetlere yol açacaktır.
Öyleyse su mikrofiltrasyonunun özelliklerine geçelim.
Mikrofiltrasyon 0,1-1 mikron büyüklüğündeki parçacıkları uzaklaştırdığı için şunu söyleyebiliriz: mikrofiltrasyon 0,1-1 mikron gözenek hücre çapına sahip membran elekler üzerinde meydana gelen su arıtmaya yönelik membran teknolojisidir. Yani bu tür membranlarda 0,5-1 mikrondan büyük tüm maddeler uzaklaştırılır:
Bunların ne kadar tamamen ortadan kaldırıldığı gözeneklerin çapına ve örneğin bakterilerin gerçek boyutuna bağlıdır. Yani bakteri uzun ama ince ise mikrofiltrasyon zarının gözeneklerinden kolayca geçecektir. Ve daha kalın küresel bakteri "eleğin" yüzeyinde kalacaktır.
Mikrofiltrasyonun en yaygın kullanımı gıda endüstrisinde(sütün yağını almak, meyve sularını konsantre etmek için) ve tıpta(tıbbi hammaddelerin birincil hazırlanması için). Mikrofiltrasyon da kullanılıyor endüstriyel içme suyu arıtımında- çoğunlukla Batı ülkelerinde (örneğin Paris'te). Moskova'daki su arıtma tesislerinden birinin de mikrofiltrasyon teknolojisini kullandığına dair söylentiler olsa da. Belki de bu doğrudur :)
Ancak mikrofiltrasyona dayalı ev filtreleri de vardır.
En yaygın örnek mikrofiltrasyon membranlarını takip edin. "İz" kelimesinden gelen iz, yani iz ve bu isim, bu tür zarların nasıl yapıldığıyla ilişkilidir. Prosedür çok basittir:
- Polimer film, kendi yüksek enerjileri nedeniyle filmdeki izleri yakan parçacıklar tarafından bombardıman edilir - yüzeyin bombardıman edildiği parçacıklar aynı boyutta olduğundan yaklaşık olarak aynı boyutta çöküntüler.
- Daha sonra bu polimer film, örneğin asit gibi bir çözelti içine kazınır, böylece parçacık darbelerinin izleri ortaya çıkar.
- O zaman polimer filmi alt tabakaya kurutmak ve sabitlemek için basit bir prosedür - işte bu, mikrofiltrasyon membranı hazır!
Sonuç olarak bu membranlar diğer membranlı su arıtma sistemlerine göre sabit gözenek çapına ve düşük gözenekliliğe sahiptir. Ve sonuç: Bu zarlar yalnızca belirli büyüklükteki parçacıkları kaldıracaktır.

Ayrıca mikrofiltrasyon ev membranlarının daha karmaşık bir versiyonu da vardır - aktif karbonla kaplanmış mikrofiltrasyon membranları. Yani, yukarıda listelenen adımlar bir adım daha içerir - ince bir tabaka uygulanması. Bu membranlar yalnızca bakterileri ve mekanik yabancı maddeleri gidermekle kalmaz, aynı zamanda
- koku,
- organik madde,
- vesaire.
Mikrofiltrasyon membranları için dikkate alınmalıdır. tehlike var. Böylece membrandan geçemeyen bakteriler bu zar üzerinde yaşamaya başla ve sorun hayatınızın ürünleri arıtılmış suya. Yani ortaya çıkıyor ikincil su zehirlenmesi. Bunu önlemek için, membranların düzenli dezenfeksiyonu konusunda üreticinin talimatlarına uymak gerekir.
İkinci tehlike ise bakteriler bu zarları kendi başlarına yemeye başlayacaklar. Ve içlerinde, zarın tutması gereken maddelerin geçmesine izin verecek kadar büyük delikler açacaklar. Bunun olmasını önlemek için bakterilere dirençli maddelere dayalı filtreler (örneğin, seramik mikrofiltrasyon membranları) satın almalı veya mikrofiltrasyon membranlarını sık sık değiştirmeye hazır olmalısınız.
Mikrofiltrasyon membranlarının sık sık değiştirilmesi de teşvik edilmektedir. yıkama mekanizması ile donatılmamış. Ve zarın gözenekleri kirle tıkanmıştır. Membranlar başarısız olur.
Prensip olarak her şey mikrofiltrasyonla ilgilidir. Mikrofiltrasyon oldukça kaliteli bir su arıtma yöntemidir. Fakat,
Mikrofiltrasyonun asıl amacı, suyu içmeye hazırlamak değil (bakteriyel kirlenme tehlikesi nedeniyle), sonraki aşamalardan önce suyu ön arıtmaya tabi tutmaktır.
Mikrofiltrasyon aşaması, sonraki su arıtma aşamalarından kaynaklanan yükün çoğunu ortadan kaldırır.

Malzemelere göre Su filtresi nasıl seçilir: http://voda.blox.ua/2008/07/Kak-vybrat-filtr-dlya-vody-22.html
« Fizik - 10. sınıf"
Moleküler fizik hangi fiziksel nesneleri (sistemleri) inceliyor?
Mekanik ve termal olaylar arasında nasıl ayrım yapılır?
Maddenin yapısının moleküler kinetik teorisi üç ifadeye dayanmaktadır:
1) madde parçacıklardan oluşur;
2) bu parçacıklar rastgele hareket eder;
3) parçacıklar birbirleriyle etkileşime girer.
Her ifade deneylerle kesinlikle kanıtlanmıştır.
İstisnasız tüm cisimlerin özellikleri ve davranışları, birbirleriyle etkileşime giren parçacıkların hareketi ile belirlenir: moleküller, atomlar ve hatta daha küçük oluşumlar - temel parçacıklar.
Molekül boyutlarının tahmini. Moleküllerin varlığından tam olarak emin olmak için boyutlarının belirlenmesi gerekir. Bunu yapmanın en kolay yolu zeytinyağı gibi bir damla yağın su yüzeyine yayılmasını izlemektir. Yeterince geniş bir kap alırsak petrol hiçbir zaman tüm yüzeyi kaplamayacaktır (Şekil 8.1). Hacmi 1 mm2 olan bir damlacığı, 0,6 m2'den fazla bir yüzey alanı kaplayacak şekilde yayılmaya zorlamak imkansızdır. Petrolün maksimum alanına yayıldığında tek molekül kalınlığında bir katman, yani “monomoleküler katman” oluşturduğunu varsayalım. Bu tabakanın kalınlığını belirlemek ve dolayısıyla zeytinyağı molekülünün boyutunu tahmin etmek kolaydır.
Yağ tabakasının hacmi V, yüzey alanı S ile tabakanın kalınlığı d'nin çarpımına eşittir, yani V = Sd. Bu nedenle zeytinyağı molekülünün doğrusal boyutu şöyledir:

Modern cihazlar, tek tek atomları ve molekülleri görmeyi ve hatta ölçmeyi mümkün kılar. Şekil 8.2, tümseklerin bireysel silikon atomları olduğu bir silikon tabakanın yüzeyinin bir mikrografını göstermektedir. Bu tür görüntüler ilk kez 1981'de karmaşık tünel mikroskopları kullanılarak elde edildi.
Zeytinyağı da dahil olmak üzere moleküllerin boyutları atomların boyutlarından daha büyüktür. Herhangi bir atomun çapı yaklaşık 10-8 cm'dir. Bu boyutlar o kadar küçüktür ki hayal edilmesi zordur. Bu gibi durumlarda karşılaştırmalara başvururlar.
İşte onlardan biri. Parmaklarınızı yumruk şeklinde sıkarsanız ve onu küre boyutuna kadar büyütürseniz, aynı büyütmedeki atom yumruk boyutuna gelecektir.
Molekül sayısı.
Çok küçük boyutlardaki moleküller nedeniyle herhangi bir makroskobik cisimdeki sayıları çok büyüktür. Kütlesi 1 g ve dolayısıyla hacmi 1 cm3 olan bir su damlasındaki yaklaşık molekül sayısını hesaplayalım.
Bir su molekülünün çapı yaklaşık 3 10 -8 cm'dir. Yoğun bir molekül paketine sahip her su molekülünün (3 10 -8 cm) 3 hacim kapladığını dikkate alırsak, bir damladaki molekül sayısını bulabilirsiniz. damlanın hacminin (1 cm3) molekül başına hacme bölünmesi:
Moleküllerin kütlesi.
Bireysel moleküllerin ve atomların kütleleri çok küçüktür. 1 gr suyun 3,7 10 22 molekül içerdiğini hesapladık. Bu nedenle, bir su molekülünün (H 2 0) kütlesi şuna eşittir:
Diğer maddelerin molekülleri, büyük organik madde molekülleri hariç, aynı düzende bir kütleye sahiptir; örneğin proteinler, tek tek atomların kütlesinden yüzbinlerce kat daha büyük bir kütleye sahiptir. Ancak yine de makroskobik ölçekte (gram ve kilogram) kütleleri son derece küçüktür.
Bağıl molekül ağırlığı.
Moleküllerin kütleleri çok küçük olduğundan hesaplamalarda mutlak kütle değerleri yerine bağıl kütle değerlerinin kullanılması daha uygundur.
Uluslararası anlaşmaya göre, tüm atomların ve moleküllerin kütleleri, bir karbon atomunun kütlesiyle (atom kütlelerinin karbon ölçeği olarak adlandırılan) karşılaştırılmaktadır.
Bir maddenin bağıl moleküler (veya atomik) kütlesi Mr, belirli bir maddenin bir molekülünün (veya atomunun) m0 kütlesinin bir karbon atomunun kütlesine oranıdır:
Tüm kimyasal elementlerin bağıl atom kütleleri doğru bir şekilde ölçülmüştür. Bir maddenin molekülünü oluşturan elementlerin bağıl atom kütlelerini toplayarak maddenin bağıl moleküler kütlesini hesaplayabiliriz. Örneğin, karbon dioksit C02'nin bağıl moleküler kütlesi yaklaşık olarak 44'e eşittir, çünkü karbonun bağıl atom kütlesi neredeyse 12'ye eşittir ve oksijen yaklaşık 16: 12 + 2 · 16 = 44'tür.
Atom ve moleküllerin karbon atomunun kütlesiyle karşılaştırılması 1961 yılında benimsendi. Bu seçimin ana nedeni, karbonun çok sayıda farklı kimyasal bileşikte bulunmasıdır. Çarpan, atomların bağıl kütlelerinin tam sayılara yakın olacağı şekilde tanıtıldı.
Suyun molar kütlesi:
Bir sıvıdaki moleküller sıkı bir şekilde paketlenirse ve her biri hacmi 100 gram olan bir küpün içine sığarsa V1 kaburga ile D, O .
Bir molekülün hacmi: burada: VM bir dua, Yok- Avogadro'nun numarası.
Bir mol sıvının hacmi: , burada: M- molar kütlesi yoğunluğudur.
Molekül Çapı:
Hesapladığımızda: 
Alüminyumun bağıl molekül ağırlığı Mr=27. Ana moleküler özelliklerini belirleyin.
1. Alüminyumun molar kütlesi: M=Bay. 10-3M = 27 . 10 -3
Normal koşullar altında (p = 10 5 Pa, T = 273 K) helyum moleküllerinin konsantrasyonunu (M = 4,10 -3 kg/mol), ortalama karekök hızlarını ve gaz yoğunluğunu bulun.Hacmi iki katına çıkarsa hava kabarcığı bir su kütlesinin hangi derinliğinden yukarı doğru yüzer? Baloncuğun içindeki havanın sıcaklığının aynı kalıp kalmadığını bilmiyoruz. Aynıysa, yükselme süreci denklemle tanımlanır. pV=sabit . Eğer değişirse, o zaman denklem.
pV/T=sabit
Sıcaklık değişimini ihmal edersek büyük bir hata yapıp yapmadığımızı değerlendirelim. En olumsuz sonuca ulaştığımızı varsayalım. Hava çok sıcak olsun ve rezervuar yüzeyindeki su sıcaklığı +25 0 C'ye (298 K) ulaşsın. Altta sıcaklık +4 0 C'den (277 K) düşük olamaz çünkü bu sıcaklık suyun maksimum yoğunluğuna karşılık gelir. Böylece sıcaklık farkı 21K olur. Başlangıç sıcaklığına göre bu değer %%'dir. Yüzeyi ile tabanı arasındaki sıcaklık farkı bu değere eşit olan böyle bir su kütlesiyle karşılaşmamız pek olası değildir. Ek olarak, kabarcık oldukça hızlı bir şekilde yüzer ve yükseliş sırasında tamamen ısınmak için zamanının olması pek olası değildir. Böylece gerçek hata önemli ölçüde daha küçük olacaktır ve kabarcıktaki hava sıcaklığındaki değişimi tamamen ihmal edebiliriz ve süreci tanımlamak için Boyle-Mariotte yasasını kullanabiliriz:, p 1 V 1 =p 2 V 2 Nerede: sayfa 1 - baloncuğun derinliklerindeki hava basıncı h (p 1 = p atm. + rgh), p 2 - yüzeye yakın baloncuğun içindeki hava basıncı.
 |
p 2 = p atm.
|
Ters çevrilmiş bir bardak bir havuza daldırılıyor. Cam hangi derinlikte batmaya başlayacak?
Ters çevrilmiş bir bardakta hava bloke edilir. Sorun, camın yalnızca belirli bir derinlikte batmaya başlamasıdır. Görünüşe göre, eğer belirli bir kritik derinlikten daha düşük bir derinliğe bırakılırsa, yukarı doğru yüzecektir (camın kesinlikle dikey olarak konumlandırıldığı ve devrilmediği varsayılarak).
Camın üzerinde yüzdüğü ve altında battığı seviye, cama farklı yönlerden uygulanan kuvvetlerin eşitliği ile karakterize edilir.
Cama düşey yönde etki eden kuvvetler, aşağıya doğru yönlendirilen yerçekimi kuvveti ve yukarıya doğru yönlendirilen kaldırma kuvvetidir.
Bir cama etki eden yer çekimi kuvveti, camın kütlesiyle doğru orantılıdır.
Sorunun bağlamından, cam battıkça yukarıya doğru kuvvetin azaldığı sonucu çıkmaktadır. Kaldırma kuvvetindeki bir azalma, yalnızca yer değiştiren sıvının hacmindeki bir azalma nedeniyle meydana gelebilir, çünkü sıvılar pratik olarak sıkıştırılamaz ve suyun yüzeydeki ve bazı derinliklerdeki yoğunluğu aynıdır.
Cam içindeki havanın sıkışması nedeniyle yer değiştiren sıvının hacminde bir azalma meydana gelebilir ve bu da basınçtaki bir artış nedeniyle meydana gelebilir. Sonucun çok yüksek doğruluğuyla ilgilenmiyorsak, cam suya daldırıldığında sıcaklıktaki değişiklik göz ardı edilebilir. İlgili gerekçe önceki örnekte verilmiştir.
Sabit sıcaklıkta gaz basıncı ile hacmi arasındaki ilişki Boyle-Mariotte yasası ile ifade edilir.
Sıvının basıncı aslında derinlikle birlikte artar ve yukarı dahil her yöne eşit şekilde iletilir.
Hidrostatik basınç, sıvının yoğunluğu ve yüksekliği (daldırma derinliği) ile doğru orantılıdır.
Camın denge durumunu karakterize eden denklemi ilk denklem olarak yazdıktan, problemin analizi sırasında bulunan ifadeleri sırayla yerine koyarak ve elde edilen denklemi istenen derinlik için çözerek, şu sonuca varıyoruz: Sayısal bir cevap elde etmek için suyun yoğunluğu, atmosferik basınç, cam kütlesi, hacmi ve serbest düşme ivmesi değerlerini bilmemiz gerekiyor.
Gerçekleştirilen tüm argümanlar aşağıdaki gibi görüntülenebilir:
![]()
![]()

Sorunun metninde veri bulunmadığından kendimiz belirleyeceğiz.
Verilen:
Suyun yoğunluğu r=10 3 kg/m3.
Atmosfer basıncı 10 5 Pa.
Cam hacmi 200 ml = 2 00. 10-3 l = 2. 10 -4 m3.
Camın kütlesi 50 gr = 5'tir. 10-2 kg.
Yerçekimi ivmesi g = 10 m/s2 .
Sayısal çözüm:

|
Balonun yükselmesi problemi de tıpkı camın batması problemi gibi statik bir problem olarak sınıflandırılabilir.
Bu cisimlere uygulanan ve yukarı-aşağı yönlendirilen kuvvetlerin eşitliği bozulduğu anda top da bardağın batması gibi yükselmeye başlayacaktır. Top da tıpkı cam gibi aşağıya doğru yönlendirilen yer çekimi kuvvetine ve yukarıya doğru yönlendirilen kaldırma kuvvetine maruz kalmaktadır.
Kaldırma kuvveti, topu çevreleyen soğuk havanın yoğunluğuyla ilgilidir. Bu yoğunluk Mendeleev-Clapeyron denkleminden bulunabilir.
Yer çekimi kuvveti topun kütlesiyle doğru orantılıdır. Topun kütlesi ise kabuğun kütlesinden ve içindeki sıcak havanın kütlesinden oluşur. Sıcak havanın kütlesi Mendeleev-Clapeyron denkleminden de bulunabilir.
Şematik olarak gerekçe şu şekilde gösterilebilir:
![]()

Denklemden istenilen miktarı ifade edebilir, problemin sayısal çözümünü elde etmek için gerekli olan miktarların olası değerlerini tahmin edebilir, bu miktarları elde edilen denklemde yerine koyabilir ve cevabı sayısal biçimde bulabilirsiniz.
Kapalı bir kapta 200 gr helyum bulunur. Gaz karmaşık bir süreçten geçer. Parametrelerindeki değişiklik, hacmin mutlak sıcaklığa karşı grafiğine yansır.1. Gazın kütlesini SI cinsinden ifade edin.
2. Bu gazın bağıl moleküler kütlesi nedir?
3. Bu gazın molar kütlesi nedir (SI cinsinden)?
4. Kabın içerdiği madde miktarı nedir?
5. Kapta kaç tane gaz molekülü var?
6. Bu gazın bir molekülünün kütlesi nedir?
7. Bölüm 1-2, 2-3, 3-1'deki süreçleri adlandırın.
8. 1,2, 3, 4 noktalarındaki gazın hacmini ml, l, m3 cinsinden belirleyin.
9. 0 C, K'de 1,2, 3, 4 noktalarındaki gaz sıcaklığını belirleyin.
10. 1, 2, 3, 4 noktalarındaki gaz basıncını mm cinsinden belirleyin. Hg Sanat. , ATM, Pa.
11. Bu süreci basınç-mutlak sıcaklık grafiği üzerinde gösterin.
12. Bu süreci basınç-hacim grafiği üzerinde gösterin.
Çözüm için talimatlar:
1. Duruma bakınız.
2. Bir elementin bağıl molekül ağırlığı periyodik tablo kullanılarak belirlenir.
3. M=Bay·10 -3 kg/mol.
7. P=const - izobarik; V=sabit-izokorik; T=sabit - izotermal.
8. 1 m3 = 10 3 l; 1 l = 10 3 ml. 9. T=t+ 273. 10. 1 atm. = 10 5 Pa = 760 mm Hg. Sanat.
8-10. Mendeleev-Clapeyron denklemini veya Boyle-Mariotte, Gay-Lussac, Charles'ın gaz yasalarını kullanabilirsiniz.
Sorunun yanıtları
| m = 0,2 kg | |||||||
| M r = 4 | |||||||
| M = 4 · 10 -3 kg/mol | |||||||
| n = 50 mol | |||||||
| N = 3 10 25 | |||||||
| m =6,7 10 -27 kg | |||||||
| 1 - 2 - izobarik | |||||||
| 2 - 3 - izokorik | |||||||
| 3 - 1 - izotermal | |||||||
| № | ml | ben | m3 | ||||
| 2 10 5 | 0,2 | ||||||
| 7 10 5 | 0,7 | ||||||
| 7 10 5 | 0,7 | ||||||
| 4 10 5 | 0,4 | ||||||
| № | 0°C | İLE | |||||
| № | mmHg | ATM | Pa | ||||
| 7,6 10 3 | 10 6 | ||||||
| 7,6 10 3 | 10 6 | ||||||
| 2,28 10 3 | 0,3 10 6 | ||||||
| 3,8 10 3 | 0,5 10 6 | ||||||
 |
 |
||||||

 ,
, ,
,






