Anglies monoksidas, anglies monoksidas (CO) yra bespalvės, bekvapės, beskonės dujos, kurios yra šiek tiek mažiau tankios nei oras. Jis toksiškas hemoglobiną gaminantiems gyvūnams (įskaitant žmones), kai koncentracija viršija maždaug 35 ppm, nors jis taip pat susidaro normalios gyvūnų metabolizmo metu. nedideli kiekiai, ir manoma, kad kai kurie normalūs biologines funkcijas. Atmosferoje jis yra kintantis erdvėje ir greitai irstantis bei turi įtakos ozono susidarymui žemės lygyje. Anglies monoksidas susideda iš vieno anglies atomo ir vieno deguonies atomo, sujungto triguba jungtimi, kurią sudaro dvi kovalentinės jungtys ir viena kovalentinė jungtis. Tai paprasčiausias anglies monoksidas. Jis yra izoelektroninis su cianido anijonu, nitrozonio katijonu ir molekuliniu azotu. Koordinavimo kompleksuose anglies monoksido ligandas vadinamas karbonilu.
Istorija
Aristotelis (384–322 m. pr. Kr.) pirmą kartą aprašė anglies deginimo procesą, dėl kurio susidaro toksiški dūmai. Senovėje buvo egzekucijos būdas – užrakinti nusikaltėlį vonioje su smilkstančiomis anglimis. Tačiau tuo metu mirties mechanizmas buvo neaiškus. Graikų gydytojas Galenas (129–199 m. po Kr.) teigė, kad pasikeitė oro sudėtis, o tai pakenkė žmonėms. 1776 metais prancūzų chemikas de Lassonne gamino CO kaitindamas cinko oksidą koksu, tačiau mokslininkas padarė klaidingą išvadą, kad dujinis produktas buvo vandenilis, nes degė mėlyna liepsna. Škotijos chemikas Williamas Cumberlandas Cruikshankas 1800 m. nustatė, kad dujos yra anglies ir deguonies turintis junginys. Jo toksiškumą šunims apie 1846 m. kruopščiai ištyrė Claude'as Bernardas. Antrojo pasaulinio karo metu mechaninei priežiūrai buvo naudojamas dujų mišinys su anglies monoksidu transporto priemonių, veikiantis kai kuriose pasaulio vietose, kur buvo mažai benzino ir dyzelino. Buvo sumontuoti išoriniai (su kai kuriomis išimtimis) medžio anglies arba medienos dujofikatoriai, į dujų maišytuvą įvedamas atmosferinio azoto, anglies monoksido ir nedidelių kiekių kitų dujofikavimo dujų mišinys. Šio proceso metu susidarantis dujų mišinys yra žinomas kaip medienos dujos. Anglies monoksidas taip pat buvo naudojamas dideliu mastu per holokaustą kai kuriose vokiečių kalbose nacių stovyklos mirtis, akivaizdžiausia dujų furgonuose Chelmne ir T4 „eutanazijos“ žudymo programoje.
Šaltiniai
Anglies monoksidas susidaro dalinai oksiduojant anglies turinčius junginius; jis susidaro, kai nepakanka deguonies susidaryti anglies dioksidui (CO2), pvz., kai veikia viryklė arba variklis vidaus degimas, V uždara erdvė. Esant deguoniui, įskaitant jo koncentraciją atmosferoje, anglies monoksidas dega mėlyna liepsna ir susidaro anglies dvideginio. Anglies dujose, kurios iki septintojo dešimtmečio buvo plačiai naudojamos patalpų apšvietimui, maisto ruošimui ir šildymui, buvo anglies monoksidas kaip svarbi kuro sudedamoji dalis. Kai kurie šiuolaikinių technologijų procesai, pavyzdžiui, geležies lydymas, vis dar gamina anglies monoksidą kaip šalutinį produktą. Pasaulyje yra didžiausi anglies monoksido šaltiniai natūralių šaltinių, dėl nuotraukos cheminės reakcijos troposferoje, kurios per metus išskiria apie 5 × 1012 kg anglies monoksido. Kiti natūralūs CO šaltiniai yra ugnikalniai, miškų gaisrai ir kitos degimo formos. Biologijoje anglies monoksidas natūraliai susidaro veikiant hemo oksigenazei 1 ir hemo 2, skaidant hemoglobiną. Šis procesas normaliems žmonėms gamina tam tikrą karboksihemoglobino kiekį, net jei jie neįkvepia anglies monoksido. Nuo tada, kai 1993 m. pirmą kartą buvo pranešta, kad anglies monoksidas yra normalus neurotransmiteris, taip pat viena iš trijų dujų, kurios natūraliai moduliuoja uždegiminius organizmo atsakus (kitos dvi yra azoto oksidas ir vandenilio sulfidas), anglies monoksidas didelis dėmesys mokslininkai kaip biologinis reguliatorius. Daugelyje audinių visos trys dujos veikia kaip priešuždegiminės medžiagos, kraujagysles plečiančios ir neovaskulinio augimo skatintojai. Tebevyksta klinikiniai nedidelio anglies monoksido kiekių, kaip vaisto, tyrimai. Tačiau per didelis anglies monoksido kiekis sukelia apsinuodijimą anglies monoksidu.
Molekulinės savybės
Anglies monoksido molekulinė masė yra 28,0, todėl jis yra šiek tiek lengvesnis už orą, kurio vidutinė molekulinė masė yra 28,8. Pagal įstatymą idealios dujos, todėl CO tankis yra mažesnis nei oro. Ryšio ilgis tarp anglies atomo ir deguonies atomo yra 112,8 pm. Šis jungties ilgis atitinka trigubą ryšį, kaip ir molekuliniame azote (N2), kurio jungties ilgis yra panašus ir molekulinė masė beveik tokia pati. Anglies ir deguonies dvigubos jungtys yra daug ilgesnės, pavyzdžiui, formaldehido 120,8 m. Virimo temperatūra (82 K) ir lydymosi temperatūra (68 K) yra labai panaši į N2 (atitinkamai 77 K ir 63 K). Ryšio disociacijos energija 1072 kJ/mol yra stipresnė nei N2 (942 kJ/mol) ir yra stipriausia žinoma cheminė jungtis. Anglies monoksido pagrindo elektronų būsena yra vienguba, nes nėra nesuporuotų elektronų.
Klijavimo ir dipolio momentas
Anglis ir deguonis kartu turi viso, 10 elektronų valentiniame apvalkale. Pagal anglies ir deguonies okteto taisyklę, du atomai sudaro trigubą ryšį, o šeši elektronai dalijasi trijose jungiančiose molekulinėse orbitalėse, o ne įprasta. dviguba jungtis, kaip ir organiniai karbonilo junginiai. Kadangi keturi iš bendrų elektronų yra iš deguonies atomo ir tik du iš anglies, vieną jungiamąją orbitą užima du elektronai iš deguonies atomų, sudarydami datyvinį arba dipolinį ryšį. Tai veda prie molekulės C←O poliarizacijos, su maža neigiamas krūvis ant anglies ir nedidelio teigiamo deguonies krūvio. Kitos dvi jungiamosios orbitalės užima po vieną elektroną iš anglies ir vieną iš deguonies, sudarydamos (polinį) kovalentiniai ryšiai su atvirkštine C → O poliarizacija, nes deguonis yra labiau elektronegatyvus nei anglis. Laisvame anglies monokside grynasis neigiamas krūvis δ- lieka anglies gale, o molekulės dipolio momentas yra mažas – 0,122 D. Taigi molekulė yra asimetrinė: deguonis turi didesnį elektronų tankį nei anglis, taip pat mažas teigiamas krūvis, palyginti su anglimi, kuris yra neigiamas. Priešingai, izoelektroninė diazoto molekulė neturi dipolio momento. Jei anglies monoksidas veikia kaip ligandas, dipolio poliškumas gali pasikeisti esant grynajam neigiamam krūviui deguonies gale, priklausomai nuo koordinacinio komplekso struktūros.
Ryšio poliškumas ir oksidacijos būsena
Teoriniai ir eksperimentiniai tyrimai parodyti, kad nepaisant didesnio deguonies elektronegatyvumo, dipolio momentas atsiranda nuo neigiamo anglies galo iki teigiamesnio deguonies galo. Šios trys jungtys iš tikrųjų yra polinės kovalentinės jungtys, kurios yra labai poliarizuotos. Apskaičiuota deguonies atomo poliarizacija yra 71% σ ryšiui ir 77% abiem π ryšiams. Anglies oksidacijos laipsnis į anglies monoksidą kiekvienoje iš šių struktūrų yra +2. Jis apskaičiuojamas taip: visi jungiantys elektronai laikomi priklausančiais labiau elektronegatyviems deguonies atomams. Tik du nesusiejantys elektronai ant anglies priskiriami anglims. Šiuo skaičiavimu anglies molekulėje yra tik du valentiniai elektronai, palyginti su keturiais laisvajame atome.
Biologinės ir fiziologinės savybės
Toksiškumas
Apsinuodijimas anglies monoksidu yra labiausiai paplitęs mirtinas apsinuodijimas oru daugelyje šalių. Anglies monoksidas yra bespalvė, bekvapė, beskonė, bet labai toksiška medžiaga. Jis jungiasi su hemoglobinu ir gamina karboksihemoglobiną, kuris „uzurpuoja“ hemoglobino vietą, kuri paprastai perneša deguonį, bet neefektyviai tiekia deguonį į organizmo audinius. Net 667 ppm koncentracija gali sukelti iki 50% organizmo hemoglobino pavertimą karboksihemoglobinu. 50% karboksihemoglobino kiekis gali sukelti traukulius, komą ir mirtį. Jungtinėse Valstijose Darbo departamentas riboja ilgalaikį anglies monoksido poveikį darbo vietoje iki 50 dalių milijonui. Per trumpą laiką anglies monoksido absorbcija yra kumuliacinė, nes gryname ore jo pusinės eliminacijos laikas yra apie 5 valandas. Dažniausi apsinuodijimo anglies monoksidu simptomai gali būti panašūs į kitus apsinuodijimo ir infekcijų tipus ir apima tokius simptomus kaip galvos skausmas, pykinimas, vėmimas, galvos svaigimas, nuovargis ir silpnumo jausmas. Nukentėjusios šeimos dažnai mano, kad yra apsinuodijusios maistu. Kūdikiai gali būti irzlūs ir blogai valgyti. Neurologiniai simptomai yra sumišimas, dezorientacija, neryškus matymas, sinkopė (sąmonės netekimas) ir traukuliai. Kai kurie apsinuodijimo anglies monoksidu aprašymai apima tinklainės kraujavimą, taip pat nenormalią vyšnių raudonumo spalvą kraujyje. Daugumoje klinikinių diagnozių šie požymiai pastebimi retai. Vienas iš šio „vyšninio“ efekto naudingumo sunkumų yra tai, kad jis koreguoja arba maskuoja, kitaip nesveika. išvaizda, nes pagrindinis veninio hemoglobino pašalinimo poveikis yra tas, kad pasmaugtas žmogus atrodo normalesnis arba miręs žmogus atrodo gyvas, panašus į raudonų dažų poveikį balzamavimo kompozicijoje. Šis dažymo efektas CO užnuodytuose audiniuose, kuriuose nėra deguonies, atsiranda dėl to komerciniam naudojimui anglies monoksidas dažant mėsą. Anglies monoksidas taip pat jungiasi su kitomis molekulėmis, tokiomis kaip mioglobinas ir mitochondrijų citochromo oksidazė. Anglies monoksido poveikis gali padaryti didelę žalą širdžiai ir centrinei nervų sistema, ypač globus pallidus, jis dažnai siejamas su ilgalaikėmis lėtinėmis patologinėmis būsenomis. Anglies monoksidas gali turėti rimtų neigiamų pasekmių nėščios moters vaisiui.
Normali žmogaus fiziologija
Anglies monoksidas natūraliai gaminamas žmogaus organizme kaip signalinė molekulė. Taigi anglies monoksidas gali turėti fiziologinis vaidmuo organizme kaip neurotransmiteris arba kraujagysles atpalaiduojantis preparatas. Dėl anglies monoksido vaidmens organizme yra susiję su jo metabolizmo sutrikimais įvairių ligų, įskaitant neurodegeneraciją, hipertenziją, širdies nepakankamumą ir uždegimą.
CO veikia kaip endogeninė signalinė molekulė.
CO moduliuoja širdies ir kraujagyslių funkcijas
CO slopina trombocitų agregaciją ir sukibimą
CO gali atlikti potencialaus terapinio agento vaidmenį
Mikrobiologija
Anglies monoksidas yra metanogeninių archėjų veisimosi terpė, acetilkofermento A statybinė medžiaga. Ši tema nauja sritis bioorganometalinė chemija. Ekstremofiliniai mikroorganizmai gali metabolizuoti anglies monoksidą tokiose vietose kaip ugnikalnių šiluminės angos. Bakterijose anglies monoksidas susidaro redukuojant anglies dioksidą fermentu anglies monoksido dehidrogenaze, baltymu, kurio sudėtyje yra Fe-Ni-S. CooA yra anglies monoksido receptorių baltymas. Jo biologinio aktyvumo mastas vis dar nežinomas. Tai gali būti bakterijų ir archėjų signalizacijos kelio dalis. Jo paplitimas tarp žinduolių nenustatytas.
Paplitimas
Anglies monoksidas atsiranda įvairiose natūraliose ir dirbtinėse aplinkose.
Anglies monoksido atmosferoje yra nedideliais kiekiais, daugiausia kaip produktas vulkaninė veikla, bet taip pat yra natūralių ir žmogaus sukeltų gaisrų (pavyzdžiui, miškų gaisrų, pasėlių likučių ir cukranendrių deginimo) produktas. Deginant iškastinį kurą, taip pat susidaro anglies monoksidas. Anglies monoksidas yra ištirpęs išlydytose vulkaninėse uolienose aukšto slėgioŽemės mantijoje. Kadangi natūralūs anglies monoksido šaltiniai yra įvairūs, labai sunku tiksliai išmatuoti natūralų išmetamų dujų kiekį. Anglies monoksidas yra greitai irstančios šiltnamio efektą sukeliančios dujos, be to, jis daro netiesioginį spinduliuotę, padidindamas metano ir troposferos ozono koncentraciją cheminėmis reakcijomis su kitais atmosferos komponentais (pvz., hidroksilo radikalu, OH), kurie kitu atveju juos sunaikintų. Dėl natūralių procesų atmosferoje jis galiausiai oksiduojamas iki anglies dioksido. Anglies monoksidas atmosferoje yra trumpalaikis (vidutiniškai apie du mėnesius), ir jo koncentracija yra kintama. Veneros atmosferoje anglies monoksidas susidaro dėl anglies dioksido fotodisociacijos veikiant elektromagnetinei spinduliuotei, kurios bangos ilgis yra mažesnis nei 169 nm. Dėl savo ilgalaikio gyvybingumo vidurio troposferoje anglies monoksidas taip pat naudojamas kaip kenksmingų medžiagų srautų pernešimo žymeklis.
Miesto tarša
Anglies monoksidas yra laikinas oro teršalas kai kuriose miesto vietovėse, pirmiausia iš vidaus degimo variklių išmetimo vamzdžių (įskaitant transporto priemones, nešiojamus ir budėjimo generatorius, vejapjoves, elektrines plovimo mašinas ir kt.) ir dėl nepilno degimo įvairių kitų kuro rūšių (įskaitant medieną, anglis, anglis, nafta, parafinas, propanas, gamtinės dujos ir šiukšlės). Didelė CO tarša gali būti stebima iš kosmoso virš miestų.
Vaidmuo formuojant pažemio ozoną
Anglies monoksidas kartu su aldehidais yra dalis cheminių reakcijų ciklų, kurie sudaro fotocheminį smogą. Jis reaguoja su hidroksilo radikalu (OH), kad susidarytų radikalo tarpinis produktas HOCO, kuris greitai perneša radikalą vandenilį į O2, kad susidarytų peroksido radikalas (HO2) ir anglies dioksidas (CO2). Tada peroksido radikalas reaguoja su azoto oksidu (NO), sudarydamas azoto dioksidą (NO2) ir hidroksilo radikalą. NO 2 fotolizės būdu gamina O(3P), taip po reakcijos su O2 susidaro O3. Kadangi hidroksilo radikalas susidaro formuojantis NO2, cheminių reakcijų sekos, prasidedančios anglies monoksidu, balansas lemia ozono susidarymą: CO + 2O2 + hν → CO2 + O3 (kur hν reiškia sugertos šviesos fotoną NO2 molekulės sekoje) Nors NO2 susidarymas yra svarbus žingsnis, vedantis į ozono susidarymą žemas lygis, jis taip pat padidina ozono kiekį kitu, šiek tiek vienas kitą paneigiančiu būdu, sumažindamas NO kiekį, kuris gali reaguoti su ozonu.
Patalpų oro tarša
Uždaroje aplinkoje anglies monoksido koncentracija gali lengvai padidėti iki mirtino lygio. Vidutiniškai kasmet Jungtinėse Amerikos Valstijose miršta 170 žmonių nuo ne automobiliams skirtų plataus vartojimo prekių, gaminančių anglies monoksidą. Tačiau, Floridos sveikatos departamento duomenimis, „daugiau nei 500 amerikiečių kasmet miršta nuo atsitiktinio anglies monoksido poveikio, o dar tūkstančiams JAV reikia skubios medicininės pagalbos dėl nemirtino apsinuodijimo anglies monoksidu“. Šie gaminiai apima sugedusius kuro deginimo įrenginius, tokius kaip krosnys, viryklės, vandens šildytuvai ir dujiniai bei žibaliniai patalpų šildytuvai; mechaniškai varoma įranga, pvz., nešiojamieji generatoriai; židiniai; ir anglis, kuri deginama namuose ir kt patalpose. Amerikos apsinuodijimų kontrolės centrų asociacija (AAPCC) pranešė apie 15 769 apsinuodijimo anglies monoksidu atvejus, dėl kurių 2007 m. mirė 39 žmonės. 2005 m. CPSC pranešė apie 94 mirtis, susijusias su apsinuodijimu anglies monoksidu iš generatoriaus. Keturiasdešimt septynios iš šių mirčių įvyko dėl atšiaurių oro sąlygų, įskaitant uraganą „Katrina“, nutrūkus elektrai. Tačiau žmonės miršta nuo apsinuodijimo anglies monoksidu, kurį sukelia ne maisto produktai, tokie kaip automobiliai, palikti važiuoti garažuose prie jų namų. Ligų kontrolės ir prevencijos centrai praneša, kad kasmet keli tūkstančiai žmonių kreipiasi į greitosios medicinos pagalbos skyrių dėl apsinuodijimo anglies monoksidu.
Buvimas kraujyje
Anglies monoksidas absorbuojamas kvėpuojant ir patenka į kraują per dujų mainus plaučiuose. Jis taip pat gaminamas hemoglobino metabolizmo metu ir iš audinių patenka į kraują, todėl yra visuose normaliuose audiniuose, net jei į organizmą nepatenka per kvėpavimą. Normalus anglies monoksido kiekis kraujyje svyruoja nuo 0% iki 3%, o rūkantiems yra didesnis. Anglies monoksido kiekis negali būti įvertintas atliekant fizinį patikrinimą. Laboratoriniams tyrimams reikalingas kraujo mėginys (arterinis ar veninis) ir laboratorinis CO-oksimetro tyrimas. Be to, neinvazinis karboksihemoglobinas (SPCO) su pulsine CO oksimetrija yra veiksmingesnis nei invaziniai metodai.
Astrofizika
Už Žemės ribų anglies monoksidas yra antra pagal gausumą esanti molekulė tarpžvaigždinė terpė, po molekulinio vandenilio. Dėl savo asimetrijos anglies monoksido molekulė sukuria daug ryškesnes spektrines linijas nei vandenilio molekulė, todėl CO yra daug lengviau aptikti. Tarpžvaigždinis CO pirmą kartą buvo atrastas naudojant radijo teleskopus 1970 m. Šiuo metu tai yra dažniausiai naudojamas molekulinių dujų indikatorius galaktikų tarpžvaigždinėje terpėje, o molekulinį vandenilį galima aptikti tik naudojant ultravioletinė šviesa, kuriam reikalingas buvimas kosminiai teleskopai. Anglies monoksido stebėjimai suteikia daugiausia informacijos apie molekulinius debesis, kuriuose susidaro dauguma žvaigždžių. Beta Pictoris, antroji ryškiausia žvaigždė Pictor žvaigždyne, skleidžia infraraudonųjų spindulių perteklių, palyginti su įprastomis tokio tipo žvaigždėmis, nes šalia žvaigždės yra daug dulkių ir dujų (įskaitant anglies monoksidą).
Gamyba
Buvo sukurta daug anglies monoksido gamybos būdų.
Pramoninė gamyba
Pagrindinis pramoninis šaltinis CO yra generatoriaus dujos, daugiausia anglies monoksido ir azoto turintis mišinys, susidarantis degant angliui ore aukšta temperatūra kai yra anglies perteklius. Krosnyje oras praleidžiamas per kokso sluoksnį. Iš pradžių pagamintas CO2 subalansuojamas su likusia karšta anglimi, kad susidarytų CO2. CO2 reakcija su anglimi, kad susidarytų CO, apibūdinama kaip Buduaro reakcija. Esant aukštesnei nei 800°C temperatūrai, CO yra vyraujantis produktas:
CO2 + C → 2 CO (ΔH = 170 kJ/mol)
Kitas šaltinis yra „vandens dujos“, vandenilio ir anglies monoksido mišinys, susidarantis vykstant garų ir anglies endoterminei reakcijai:
H2O + C → H2 + CO (ΔH = +131 kJ/mol)
Iš gamtinių dujų ir kito kuro gali būti gaminamos ir kitos panašios „sintezės dujos“. Anglies monoksidas taip pat yra metalo oksido rūdų redukavimo anglimi šalutinis produktas:
MO + C → M + CO
Anglies monoksidas taip pat susidaro tiesiogiai oksiduojant anglį į ribotas kiekis deguonies ar oro.
2C (s) + O 2 → 2СО (g)
Kadangi CO yra dujos, atkūrimo procesas gali būti valdomas kaitinant, naudojant teigiamą (palankią) reakcijos entropiją. Ellinghamo diagrama rodo, kad aukštoje temperatūroje CO susidarymas yra palankesnis nei CO2.
Paruošimas laboratorijoje
Anglies monoksidą galima patogiai gauti laboratorijoje dehidratuojant skruzdžių rūgštis arba oksalo rūgštį, pavyzdžiui, naudojant koncentruotą sieros rūgštį. Kitas būdas yra šildyti vienalytis mišinys miltelių pavidalo cinko metalas ir kalcio karbonatas, kuris išskiria CO ir palieka cinko oksidą ir kalcio oksidą:
Zn + CaCO3 → ZnO + CaO + CO
Sidabro nitratas ir jodoformas taip pat gamina anglies monoksidą:
CHI3 + 3AgNO3 + H2O → 3HNO3 + CO + 3AgI
Koordinacinė chemija
Dauguma metalų sudaro koordinacinius kompleksus, kuriuose yra kovalentiškai prijungto anglies monoksido. Tik žemesnės oksidacijos būsenos metalai susijungs su anglies monoksido ligandais. Taip yra todėl, kad reikalingas pakankamas elektronų tankis, kad būtų lengviau perkelti iš metalo DXZ orbitos į π*. molekulinė orbita iš SO. Vienintelė pora ant anglies atomo CO taip pat suteikia elektronų tankį dx²-y² ant metalo, kad sudarytų sigma ryšį. Ši elektronų donorystė taip pat pasireiškia cis efektu arba CO ligandų labilizavimu cis padėtyje. Pavyzdžiui, nikelio karbonilą sudaro tiesioginis anglies monoksido ir metalo nikelio derinys:
Ni + 4 CO → Ni (CO) 4 (1 baras, 55 °C)
Dėl šios priežasties vamzdyje ar jo dalyje esantis nikelis neturėtų ilgai liestis su anglies monoksidu. Nikelio karbonilas lengvai skyla atgal į Ni ir CO, kai liečiasi su karštais paviršiais, ir šis metodas naudojamas pramoniniam nikelio valymui Mond procese. Nikelio karboniluose ir kituose karboniluose elektronų pora ant anglies sąveikauja su metalu; anglies monoksido dovanoja elektronų pora metalo. Tokiose situacijose anglies monoksidas vadinamas karbonilo ligandu. Vienas iš svarbiausių metalų karbonilų yra geležies pentakarbonilas, Fe(CO)5. Daugelis metalo-CO kompleksų gaminami dekarbonilinant organinius tirpiklius, o ne iš CO. Pavyzdžiui, iridžio trichloridas ir trifenilfosfinas reaguoja verdančiame 2-metoksietanolyje arba DMF, kad susidarytų IrCl(CO)(PPh3)2, naudojant infraraudonųjų spindulių spektroskopiją.
Organinė chemija ir pagrindinių elementų grupių chemija
Esant stiprios rūgštys ir vandens, anglies monoksidas reaguoja su alkenais ir susidaro karboksirūgštys procese, žinomame kaip Koch-Haaf reakcijos. Guttermann-Koch reakcijoje arenai paverčiami benzaldehido dariniais, esant AlCl3 ir HCl. Organiniai ličio junginiai (pavyzdžiui, butillitis) reaguoja su anglies monoksidu, tačiau šios reakcijos turi mažai mokslinio pritaikymo. Nors CO reaguoja su karbokationais ir karbanionais, jis yra santykinai neaktyvus organiniai junginiai be metalinių katalizatorių įsikišimo. Su pagrindinės grupės reagentais CO patiria keletą reikšmingų reakcijų. CO chlorinimas yra pramoninis procesas, kurio metu susidaro svarbus junginys fosgenas. Su boranu CO sudaro aduktą H3BCO, kuris yra izoelektroninis su acilu + katijonu. CO reaguoja su natriu ir sukuria produktus, gautus iš C-C jungties. Anglies monoksido polimerais gali būti laikomi junginiai cikloheksahegeksonas arba trichinoilas (C6O6) ir ciklopentanpentonas arba leukono rūgštis (C5O5), kurių iki šiol buvo gauta tik nedideliais kiekiais. Esant didesniam nei 5 GPa slėgiui, anglies monoksidas virsta kietu anglies ir deguonies polimeru. Tai metastabili medžiaga atmosferos slėgis, bet tai galingas sprogmuo.
Naudojimas
Chemijos pramonė
Anglies monoksidas yra pramoninės dujos, kurios gali būti plačiai naudojamos birių cheminių medžiagų gamyboje. Dideli kiekiai aldehidai susidaro vykstant alkenų, anglies monoksido ir H2 hidroformilinimo reakcijai. Hidroformilinimas Shell procese leidžia sukurti ploviklio pirmtakus. Fosgenas, naudingas izocianatams, polikarbonatams ir poliuretanams gaminti, gaunamas praleidžiant išvalytą anglies monoksidą ir chloro dujos per porėtos aktyvintos anglies sluoksnį, kuris tarnauja kaip katalizatorius. Pasaulinė šio junginio gamyba 1989 m. buvo įvertinta 2,74 mln. tonų.
CO + Cl2 → COCl2
Metanolis gaunamas hidrinant anglies monoksidą. Susijusioje reakcijoje anglies monoksido hidrinimas apima C-C jungties susidarymą, kaip ir Fischer-Tropsch procese, kai anglies monoksidas hidrinamas iki skysto angliavandenilio kuro. Ši technologija leidžia anglį ar biomasę paversti dyzelinu. Monsanto procese anglies monoksidas ir metanolis reaguoja dalyvaujant rodžio katalizatoriui ir homogeninei jodo rūgščiai, sudarydami acto rūgštį. Šis procesas yra atsakingas už daugumą pramoninės gamybos acto rūgštis. Pramoniniu mastu grynas anglies monoksidas yra naudojamas nikeliui išvalyti Mond procese.
Mėsos dažymas
Anglies monoksidas naudojamas modifikuotame atmosferos sistemos pakuočių JAV, visų pirma į šviežios mėsos produktų, tokių kaip jautiena, kiauliena ir žuvis, pakuotes, kad būtų išlaikyta jų šviežia išvaizda. Anglies monoksidas, susijungęs su mioglobinu, sudaro karboksimioglobiną – ryškiai vyšnių raudoną pigmentą. Karboksimioglobinas yra stabilesnis nei oksiduota mioglobino forma oksimioglobinas, kuris gali oksiduotis iki rudo pigmento metmioglobino. Ši stabili raudona spalva gali išsilaikyti daug ilgiau nei įprasta supakuota mėsa. Įprasti anglies monoksido kiekiai, naudojami šį procesą naudojančiuose augaluose, yra nuo 0,4 % iki 0,5 %. JAV Maisto ir vaistų administracija (FDA) šią technologiją pirmą kartą pripažino „bendrai saugia“ (GRAS) 2002 m., kad ji būtų naudojama kaip antrinė pakavimo sistema, ir jai nereikia ženklinti. 2004 m. FDA patvirtino CO kaip pagrindinį pakavimo būdą, nurodydama, kad CO neužmaskuoja sugadintų kvapų. Nepaisant šio sprendimo, jis išlieka prieštaringas klausimas apie tai, ar šis metodas užmaskuoja maisto gedimą. 2007 m. JAV Atstovų Rūmuose buvo pasiūlytas įstatymo projektas, kuriuo modifikuotas anglies monoksido pakavimo procesas būtų pavadintas spalvotu priedu, tačiau įstatymo projektas nebuvo priimtas. Šis pakavimo procesas yra uždraustas daugelyje kitų šalių, įskaitant Japoniją, Singapūrą ir Europos Sąjungą.
Vaistas
Biologijoje anglies monoksidas natūraliai susidaro veikiant hemo oksigenazei 1 ir hemo 2, skaidant hemoglobiną. Šis procesas normaliems žmonėms gamina tam tikrą karboksihemoglobino kiekį, net jei jie neįkvepia anglies monoksido. Nuo tada, kai 1993 m. pirmą kartą buvo pranešta, kad anglies monoksidas yra normalus neuromediatorius, taip pat viena iš trijų dujų, kurios natūraliai moduliuoja uždegiminius organizmo atsakus (kitos dvi yra azoto oksidas ir vandenilio sulfidas), anglies monoksidas sulaukė didelio klinikinio dėmesio kaip biologinis. reguliatorius. Yra žinoma, kad daugelyje audinių visos trys dujos veikia kaip priešuždegiminės medžiagos, kraujagysles plečiančios ir neovaskulinio augimo skatintojai. Tačiau šios problemos yra sudėtingos, nes neovaskulinis augimas ne visada yra naudingas, nes jis turi įtakos naviko augimui, taip pat šlapios geltonosios dėmės degeneracijos vystymuisi – ligai, kurios rizika rūkant padidėja 4–6 kartus (pagrindinis šaltinis). anglies monoksido kiekis kraujyje, kelis kartus daugiau nei natūralus). Egzistuoja teorija, kad kai kurių nervų ląstelių sinapsių metu, kai saugomi ilgalaikiai prisiminimai, priimančioji ląstelė gamina anglies monoksidą, kuris perduodamas atgal į siuntimo kamerą, todėl ateityje jis bus lengviau perduodamas. Nustatyta, kad kai kuriose tokiose nervų ląstelėse yra guanilato ciklazės – fermento, kurį aktyvuoja anglies monoksidas. Daugelis laboratorijų visame pasaulyje atliko tyrimus, susijusius su anglies monoksidu dėl jo priešuždegiminių ir citoprotekcinių savybių. Šios savybės gali būti naudojamos siekiant išvengti daugelio patologinių būklių, įskaitant išeminį reperfuzijos pažeidimą, transplantato atmetimą, aterosklerozę, sunkų sepsį, sunkią maliariją ar autoimunines ligas. Klinikiniai tyrimai buvo atlikti su žmonėmis, tačiau rezultatai dar nepaskelbti.
Kiekvienas, kam teko susidurti su šildymo sistemų – krosnių, katilų, katilų, vandens šildytuvų, skirtų bet kokio pavidalo buitiniam kurui – eksploatavimu, žino, koks pavojingas anglies monoksidas yra žmogui. Gana sunku jį neutralizuoti dujinėje būsenoje, nėra veiksmingų namų kovos su anglies monoksidu būdų, todėl dauguma apsaugos priemonių yra skirtos užkirsti kelią ir laiku nustatyti anglies monoksidą ore.
Toksiškos medžiagos savybės
Gamtoje ir savybėse anglies monoksido nėra nieko neįprasto. Iš esmės tai yra anglies arba anglies turinčio kuro dalinės oksidacijos produktas. Anglies monoksido formulė yra paprasta ir nesudėtinga – CO, chemiškai – anglies monoksidas. Vienas anglies atomas yra prijungtas prie deguonies atomo. Organinio kuro degimo procesų pobūdis yra toks, kad anglies monoksidas yra neatsiejama bet kokios liepsnos dalis.

Kaitinant krosnyje, anglys, susijęs kuras, durpės, malkos dujofikuojamos į anglies monoksidą ir tik tada sudeginamos pritekėjus oro. Jei anglies dioksidas iš degimo kameros nutekėjo į patalpą, jis išliks stabilios būklės iki to momento, kai anglies srautas bus pašalintas iš patalpos ventiliacijos būdu arba susikaups, užpildydamas visą erdvę, nuo grindų iki lubų. IN pastarasis atvejis Tik elektroninis anglies monoksido jutiklis gali išgelbėti situaciją, reaguodamas į menkiausią nuodingų dūmų koncentracijos padidėjimą kambario atmosferoje.
Ką reikia žinoti apie anglies monoksidą:
- Standartinėmis sąlygomis anglies monoksido tankis yra 1,25 kg/m3, o tai labai artima savitajam oro tankiui 1,25 kg/m3. Karštas ir net šiltas monoksidas lengvai pakyla iki lubų, o vėsdamas nusėda ir susimaišo su oru;
- Anglies monoksidas yra beskonis, bespalvis ir bekvapis, net ir esant didelei koncentracijai;
- Norint pradėti formuotis anglies monoksidui, pakanka metalą, besiliečiantį su anglimi, pašildyti iki 400-500 o C temperatūros;
- Dujos gali degti ore, išsiskirti didelis kiekisšilumos, maždaug 111 kJ/mol.
Pavojinga ne tik anglies monoksido įkvėpimas, bet ir dujų ir oro mišinys gali sprogti, kai tūrinė koncentracija pasiekia nuo 12,5% iki 74%. Šia prasme dujų mišinys panašus į buitinį metaną, tačiau daug pavojingesnis už tinklo dujas.

Metanas yra lengvesnis už orą ir mažiau toksiškas įkvėpus, be to, į dujų srautą įtraukus specialų priedą – merkaptaną, jo buvimą patalpoje galima lengvai aptikti pagal kvapą. Jei virtuvė šiek tiek užteršta, galite patekti į patalpą ir ją vėdinti be jokių pasekmių sveikatai.
Su anglies monoksidu viskas yra sudėtingiau. Glaudus ryšys tarp CO ir oro neleidžia veiksmingai pašalinti toksiškų dujų debesies. Atvėsus, dujų debesis pamažu nusės grindų plote. Įsijungus anglies monoksido detektoriui arba aptikus degimo produktų nuotėkį iš krosnelės ar kieto kuro katilo, būtina nedelsiant imtis vėdinimo priemonių, nes priešingu atveju pirmieji nukentės vaikai ir augintiniai.
Panaši anglies monoksido savybė anksčiau buvo plačiai naudojama kovojant su graužikais ir tarakonais, tačiau efektyvumas dujų atakažymiai mažesnis šiuolaikinėmis priemonėmis, o rizika apsinuodyti yra neproporcingai didesnė.
Jūsų informacijai!
CO dujų debesis, jei nėra ventiliacijos, ilgą laiką gali išlaikyti savo savybes nepakitusias.
Jei kyla įtarimas dėl anglies monoksido kaupimosi rūsiuose, ūkinėse patalpose, katilinėse, rūsiuose, pirmiausia reikia užtikrinti maksimalų vėdinimą, kai dujų mainų greitis yra 3-4 vnt. per valandą.
Dūmų atsiradimo patalpoje sąlygos Anglies monoksidas gali būti gaminamas naudojant daugybę cheminių reakcijų, tačiau tam reikia specifinių reagentų ir jų sąveikos sąlygų. Tokiu būdu apsinuodijimo dujomis rizika yra beveik lygus nuliui
- . Pagrindinės priežastys, dėl kurių anglies monoksidas atsiranda katilinėje ar virtuvės zonoje, išlieka du veiksniai:
- Prasta trauka ir dalinis degimo produktų srautas iš degimo šaltinio į virtuvės zoną;
- Netinkamas katilo, dujų ir krosnių įrangos veikimas;
- Plastikinių, laidų, polimerinių dangų ir medžiagų gaisrai ir vietiniai gaisrai;
Atliekos dujos iš kanalizacijos linijų.

Anglies monoksido šaltinis gali būti antrinis pelenų degimas, birių suodžių nuosėdos kaminuose, suodžiai ir derva, įterpta į židinių dangų ir suodžių gesintuvų mūrą.
Dažniausiai dujų CO šaltinis yra rūkstančios anglys, kurios, uždarius vožtuvą, išdega krosnyje. Ypač daug dujų išsiskiria termiškai skaidant malkas, kai nėra oro, maždaug pusę dujų debesies užima anglies monoksidas. Todėl bet kokie bandymai su mėsos ir žuvies rūkymu naudojant dūmus, gautus iš rusenančių drožlių, turėtų būti atliekami tik atvirame ore.

Virimo metu taip pat gali atsirasti nedidelis anglies monoksido kiekis. Pavyzdžiui, kas susidūrė su dujinių šildymo katilų su uždara pakura įrengimu virtuvėje, žino, kaip anglies monoksido davikliai reaguoja į keptas bulves ar bet kokį verdančiame aliejuje keptą maistą.
Klastingas anglies monoksido pobūdis

Pagrindinis anglies monoksido pavojus yra tas, kad neįmanoma pajusti ir nujausti jo buvimo patalpos atmosferoje tol, kol dujos su oru nepatenka į kvėpavimo sistemą ir neištirpsta kraujyje.
- Galvos skausmas, negalavimas ir mieguistumo vystymasis prasideda, kai tūrinis dujų kiekis ore yra 0,009-0,011%. Fiziškai sveikas žmogus gali atlaikyti iki trijų valandų veikiant užterštoje atmosferoje;
- Pykinimas, stiprus skausmas raumenyse, esant 0,065-0,07% koncentracijai, gali išsivystyti mėšlungis, alpimas, orientacijos praradimas. Kambaryje praleidžiamas laikas iki neišvengiamų pasekmių atsiradimo yra tik 1,5-2 valandos;
- Kai anglies monoksido koncentracija viršija 0,5%, net kelios sekundės buvimas dujomis užterštoje erdvėje reiškia mirtį.
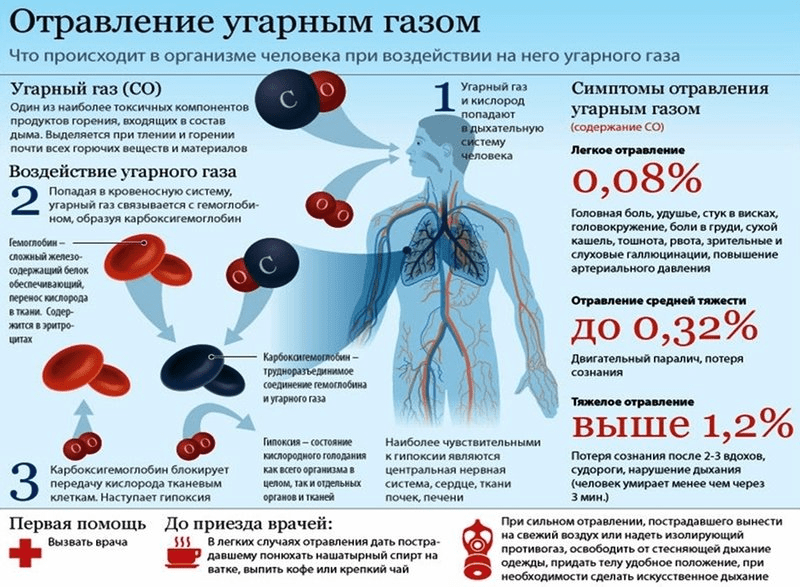
Net jei žmogus pats saugiai ištrūko iš patalpos, kurioje yra didelė anglies monoksido koncentracija, jam vis tiek reikės medicininė priežiūra ir priešnuodžių vartojimas, nes apsinuodijus kraujotakos sistema ir sutrikus kraujotakai smegenyse pasekmės vis tiek atsiras, tik kiek vėliau.
Anglies monoksido molekules gerai sugeria vanduo ir druskos tirpalai. Todėl kaip pirmoji galima apsaugos priemonė dažnai naudojami įprasti rankšluosčiai ir servetėlės, sudrėkintos bet kokiu turimu vandeniu. Tai leidžia kelioms minutėms sustabdyti anglies monoksido patekimą į jūsų kūną, kol galėsite išeiti iš kambario.
Šia anglies monoksido savybe dažnai piktnaudžiauja kai kurie šildymo įrangos, kurioje yra įmontuoti CO jutikliai, savininkai. Įsijungus jautriam jutikliui, užuot vėdinę patalpą, prietaisas dažnai tiesiog uždengiamas drėgnu rankšluosčiu. Dėl to po keliolikos tokių manipuliacijų anglies monoksido jutiklis sugenda, o apsinuodijimo rizika padidėja eilės tvarka.
Techninės anglies monoksido aptikimo sistemos
Tiesą sakant, šiandien yra tik vienas būdas sėkmingai kovoti su anglies monoksidu, naudojant specialius elektroniniai prietaisai ir jutikliai, fiksuojantys perteklinę CO koncentraciją patalpoje. Galima, žinoma, padaryti ir ką nors paprastesnio, pavyzdžiui, įsirengti galingą vėdinimą, kaip tai daro mėgstantys ilsėtis prie tikro mūrinio židinio. Tačiau tokiame sprendime yra tam tikra apsinuodijimo anglies monoksidu rizika keičiant traukos kryptį vamzdyje, be to, gyventi esant stipriai traukai taip pat nėra labai naudinga sveikatai.

Anglies monoksido jutiklio įtaisas
Anglies monoksido kiekio valdymo gyvenamųjų ir buitinių patalpų atmosferoje problema šiandien yra tokia pat aktuali kaip gaisro ar apsaugos signalizacija.
Specializuotose šildymo ir dujų įrangos parduotuvėse galite įsigyti keletą dujų kiekio stebėjimo prietaisų variantų:
- Cheminiai signalai;
- Infraraudonųjų spindulių skaitytuvai;
- Kietojo kūno jutikliai.
Jautrus prietaiso jutiklis paprastai turi elektroninę plokštę, kuri užtikrina maitinimą, kalibravimą ir signalo konvertavimą į aiški forma indikacija. Tai gali būti tiesiog žali ir raudoni šviesos diodai skydelyje, garsinė sirena, skaitmeninė informacija, skirta signalui perduoti kompiuterių tinklas arba automatinio vožtuvo valdymo impulsas, kuris išjungia tiekimą buitinės dujos prie šildymo katilo.

Akivaizdu, kad jutiklių su kontroliuojamu uždarymo vožtuvu naudojimas yra būtina priemonė, tačiau dažnai šildymo įrangos gamintojai sąmoningai sukuria „apsaugą“, kad išvengtų visokių manipuliacijų su dujų įrangos saugumu.
Cheminiai ir kietojo kūno valdymo prietaisai
Pigiausia ir prieinamiausia jutiklio versija su cheminiu indikatoriumi yra pagaminta tinklinės kolbos pavidalu, lengvai pralaidžia orui. Kolbos viduje yra du elektrodai, atskirti akyta pertvara, impregnuota šarmo tirpalu. Anglies monoksido atsiradimas sukelia elektrolito karbonizaciją, jutiklio laidumas smarkiai sumažėja, kurį elektronika iš karto nuskaito kaip pavojaus signalą. Po įdiegimo įrenginys yra įjungtas neaktyvi būsena ir neveikia tol, kol ore neatsiranda anglies monoksido pėdsakų, viršijančių leistiną koncentraciją.
Kietojo kūno jutikliuose vietoj šarmu impregnuoto asbesto gabalo naudojami dviejų sluoksnių alavo dioksido ir rutenio maišeliai. Dujų atsiradimas ore sukelia gedimą tarp jutiklio įrenginio kontaktų ir automatiškai įjungia aliarmą.

Skaitytuvai ir elektroninės apsaugos
Infraraudonųjų spindulių jutikliai, veikiantys aplinkinio oro skenavimo principu. Integruotas infraraudonųjų spindulių jutiklis suvokia lazerio šviesos diodo švytėjimą ir dujų absorbcijos intensyvumo pokyčius šiluminė spinduliuotė suaktyvinamas paleidimo įtaisas.

CO labai gerai sugeria šiluminę spektro dalį, todėl tokie įrenginiai veikia budėtojo arba skaitytuvo režimu. Nuskaitymo rezultatas gali būti rodomas kaip dviejų spalvų signalas arba anglies monoksido kiekio ore nuoroda skaitmenine arba tiesine skale.
Kuris jutiklis geresnis
Už teisingas pasirinkimas Montuojant anglies monoksido jutiklį, būtina atsižvelgti į darbo režimą ir patalpos, kurioje turi būti montuojamas jutiklis, pobūdį. Pavyzdžiui, cheminiai jutikliai, laikomi pasenusiais, puikiai veikia katilinėse ir pagalbinėse patalpose. Nebrangus anglies monoksido aptikimo įrenginys gali būti sumontuotas jūsų namuose ar dirbtuvėse. Virtuvėje tinklelis greitai pasidengia dulkėmis ir riebalų nuosėdomis, o tai smarkiai sumažina cheminio kūgio jautrumą.
Kietojo kūno anglies monoksido jutikliai vienodai gerai veikia bet kokioje aplinkoje, tačiau jiems reikia galingo išorinio maitinimo šaltinio. Prietaiso kaina yra didesnė nei cheminių jutiklių sistemų kaina.

Šiandien labiausiai paplitę infraraudonųjų spindulių jutikliai. Jie aktyviai naudojami gyvenamųjų namų individualių šildymo katilų apsaugos sistemoms komplektuoti. Tuo pačiu metu valdymo sistemos jautrumas laikui bėgant praktiškai nekinta dėl dulkių ar oro temperatūros. Be to, tokiose sistemose, kaip taisyklė, yra įmontuoti testavimo ir kalibravimo mechanizmai, kurie leidžia periodiškai tikrinti jų veikimą.
Anglies monoksido stebėjimo prietaisų montavimas
Anglies monoksido jutiklius turi montuoti ir prižiūrėti tik kvalifikuotas personalas. Periodiškai prietaisai yra tikrinami, kalibruojami, prižiūrimi ir keičiami.
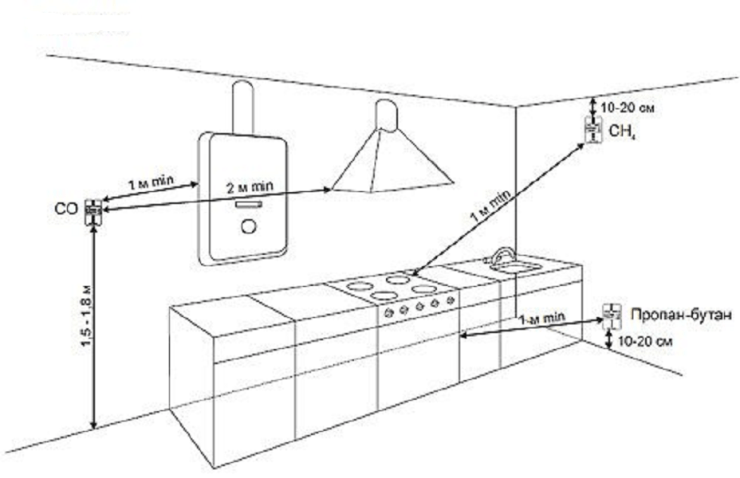
Jutiklis turi būti sumontuotas 1–4 m atstumu nuo dujų šaltinio arba nuotoliniai jutikliai montuojami 150 cm aukštyje virš grindų lygio ir turi būti sukalibruoti pagal viršutinę ir apatinę jautrumo slenksčius.
Gyvenamųjų anglies monoksido detektorių tarnavimo laikas yra 5 metai.
Išvada
Kova su anglies monoksido susidarymu reikalauja atidumo ir atsakingo požiūrio į sumontuotą įrangą. Bet kokie eksperimentai su jutikliais, ypač puslaidininkiniais, smarkiai sumažina prietaiso jautrumą, o tai galiausiai lemia anglies monoksido kiekio padidėjimą virtuvės ir viso buto atmosferoje, lėtai nuodijant visus jo gyventojus. Anglies monoksido stebėjimo problema yra tokia rimta, kad gali būti, kad jutiklių naudojimas ateityje gali būti privalomas visoms individualaus šildymo kategorijoms.
Mokslo metai jau prasidėjo, o tai reiškia, kad 9 ir 11 klasių mokiniams atėjo laikas rimtai pagalvoti apie artėjančius egzaminus. Po rimtų naujovių, su kuriomis teko susidurti praėjusių metų abiturientams, mokytojai ir būsimi stojantieji stengiasi nepraleisti svarbių naujienų apie artėjantį OGE ir valstybinį egzaminą. „Rosobrnadzor“ jau pristatė tvarkaraščio projektą Vieningi valstybiniai egzaminai ir OGE 2018 m., todėl siūlome susipažinti su labiausiai tikėtinu 9 ir 11 klasių mokinių testų tvarkaraščiu.
Baigiamasis rašinys yra pirmasis išbandymas abiturientams, svajojantiems sėkmingai įstoti į universitetą pagal biudžeto finansuojamą studijų formą. Kaip ir pagrindinių valstybinio akademinio egzamino dalykų, 2018 m. studentai turės galimybę perlaikyti rašinį, jei pirmasis bandymas bus nesėkmingas, nes Rosobrnadzor į tvarkaraščio projektą įtraukė tris oficialias datas:
- 2017 m. gruodžio 6 d.;
- 2018 m. vasario 7 d.;
- 2018 m. gegužės 16 d
Ypatingas dėmesys turėtų būti skiriamas ruošiantis tiems, kurie planuoja stoti į humanitarinius mokslus ir studijuoti dalyką „Literatūra“. Daugiau apie tai, kokios naujovės galimos, kaip vyks egzaminas ir kaip tinkamai jam pasiruošti, galite paskaityti mūsų svetainės medžiagoje.
Vieningas valstybinių egzaminų kalendorius 11 klasėms 2018 m
Kaip ir anksčiau, mokiniai egzaminus laikys trimis etapais:
- anksti;
- pagrindinis;
- papildomas.
Ankstyvasis vieningo valstybinio egzamino laikotarpis 2018 m
Ankstesnių metų abiturientai, taip pat 11 klasių mokiniai, kurie dėl svarbių priežasčių (pagrįstų dokumentais) negalės atvykti į pagrindinę Vieningojo valstybinio egzamino sesiją, turi teisę laikyti egzaminą anksčiau laiko.
Oficialiame 2018 m. valstybinio egzamino tvarkaraščio projekte siūlomos šios ankstyvojo etapo datos:
Savaitės diena | ||
geografija, informatika |
||
rusų kalba |
||
istorija, chemija |
||
matematika (bazė ir profilis) |
||
Pirmadienis | užsienio kalbos ( rašytinė dalis), biologija, fizika |
|
socialiniai mokslai, literatūra |
||
Rezervinės dienos |
||
geografija, chemija, informatika, užsienio kalbos (žodinė dalis), istorija |
||
Pirmadienis | užsienio kalbos, literatūra, fizika, socialiniai mokslai, biologija |
|
Rusų kalba, matematikos bazė ir profilis |
||
Atkreipiame dėmesį, kad norint dalyvauti ankstyvoje sesijoje reikia pateikti prašymą mokyklos direktoriui iki kovo 1 d.!
Pagrindinė 2018 m. vieningo valstybinio egzamino sesija
Dauguma 11 klasės absolventų ir būsimų kandidatų, norinčių gauti atestaciją, kad galėtų kreiptis į Rusijos universitetus, gali sutelkti dėmesį į pagrindinės sesijos datas.
Savaitės diena | ||
Pirmadienis | geografija, informatika |
|
matematika ( bazinis lygis) |
||
matematika (profilio lygis) |
||
Pirmadienis | chemija, istorija |
|
rusų kalba |
||
užsienio kalbos (žodinė dalis) |
||
užsienio kalbos (žodinė dalis) |
||
socialinis mokslas |
||
Pirmadienis | biologija, užsienio kalbos |
|
literatūra, fizika |
||
Rezervinės dienos |
||
geografija, informatika |
||
Pirmadienis | matematika (pagrindinė ir specializuota) |
|
rusų kalba |
||
istorija, chemija, biologija, užsienio kalbos |
||
literatūra, fizika, bendrasis mokslas |
||
užsienio kalbos (žodinė dalis) |
||
Pirmadienis | visi daiktai |
|
Papildomas laikotarpis (Vieningojo valstybinio egzamino perlaikymas) 2018 m
Rudens kartojimas – paskutinė galimybė gauti pažymėjimą ir įstoti į universitetą, bent jau pagal sutartį. Kai kurie universitetai pratęsia priėmimą į specialybes, kurios nėra labai populiarios tarp stojančiųjų, todėl studentu galima tapti ir po rudens perlaikymo. Daugiau apie teises į teises skaitykite atitinkamame straipsnyje mūsų informacinio portalo puslapiuose.
Rosobrnadzor patvirtintas tvarkaraščio projektas suteikia paskutinę galimybę 2018 m. laikiusiems valstybinio egzamino testą šiais skaičiais:
Savaitės diena | ||
rusų kalba |
||
matematika (pagrindinis lygis) |
||
Rezervo diena |
||
matematika (pagrindinis lygis), rusų kalba |
||
OGE kalendorius 9 klasei 2018 m
Palyginti su 11 klasių egzaminų kalendoriumi, devintokams buvo skirta daugiau dienų perlaikyti rugsėjo mėnesio egzaminą. Ir dalykų, kuriuos galima pakartoti, spektras yra daug platesnis.
Ankstyvo OGE užbaigimo datos 2018 m
Siūlomas tvarkaraščio projektas patvirtina, kad 9 klasės mokiniai, galintys anksti baigti, galės lankyti OGE 2018 m. kovo mėn. Patvirtintos šios preliminaraus posėdžio datos:
Savaitės diena | ||
matematikos |
||
Pirmadienis | ||
rusų kalba |
||
užsienio kalbų |
||
Rezervinės dienos |
||
Pirmadienis | matematikos |
|
istorija, biologija, fizika, geografija |
||
rusų kalba |
||
Pirmadienis | informatika, socialiniai mokslai, chemija, literatūra |
|
užsienio kalbų |
||
Kaip ir 11 klasių abiturientams, taip ir devintokams reikės rinkti reikalingus dokumentus, patvirtinantis būtinybę keisti egzamino laiką. Rekomenduojame vasario mėnesį šiuo klausimu kreiptis į ugdymo įstaigos direktorių ir išsiaiškinti visus svarbius niuansus.
Pagrindinis OGE 2018 etapas
Daugumai abiturientų egzaminai prasidės gegužės 25 d. su įskaitomis užsienio kalbų. Rosobrnadzor siūlo tokį pagrindinio 2018 m. OGE tvarkaraščio projektą:
Savaitės diena | ||
užsienio kalbų |
||
užsienio kalbų |
||
rusų kalba |
||
istorija, biologija, fizika, geografija |
||
fizika, informatika |
||
matematikos |
||
Rezervinės dienos |
||
Pirmadienis | istorija, biologija, fizika, geografija |
|
rusų kalba |
||
užsienio kalbų |
||
matematikos |
||
socialiniai mokslai, chemija, informatika, literatūra |
||
visi daiktai |
||

Rugsėjo mėn. OGE 2018 kartojimas
Rugsėjo sesija suteiks galimybę tiems, kurie negali išlaikyti egzamino pagrindiniu laikotarpiu dėl ligos arba gaus nepatenkinamus pažymius. Taip pat šios datos bus aktualios tiems, kurių rezultatai bus atšaukti dėl nuo jų nepriklausančių priežasčių.
Savaitės diena | ||
rusų kalba |
||
matematikos |
||
Pirmadienis | istorija, biologija, fizika, geografija |
|
socialiniai mokslai, chemija, informatika, literatūra |
||
užsienio kalbų |
||
Rezervinės dienos |
||
Pirmadienis | rusų kalba |
|
istorija, biologija, fizika, geografija |
||
matematikos |
||
socialiniai mokslai, chemija, informatika, literatūra |
||
užsienio kalbų |
||
Norėdami gauti daugiau informacijos apie tai, kas laukia studentų OGE 2018 m., skaitykite apie artėjančių naujovių mokslo metus.
„Egzaminai“ – šio žodžio bijo ne tik 11 klasių abiturientai, bet ir jaunesni. Rusijos devintokams taip pat sunku, nes mokslo metų pabaigoje specialiai sudaryta komisija patikrina jų žinių lygį pagrindiniu valstybiniu egzaminu (sutrumpintai OGE).
Būtent šis testas lemia studento likimą ir suteikia galimybę toliau mokytis 10-11 klasėse arba stoti į kolegiją (technikos mokyklą). Kiekvienas devintokas gali pradėti ruoštis egzaminui, juolab kad jau žinoma, kurią dieną vyks OGE 2018.
Tik atrodo, kad iki mokslo metų pabaigos dar toli. Tiesą sakant, laikas bėgs nepastebimai ir tik tikrai pasiruošę studentai galės išlaikyti egzaminą įvertinimu „Puikiai“.
O gal OGE bus atšauktas?
Ši mintis metai iš metų slysta 9 klasės mokinių galvose. Žinoma, vaikinai panašus sprendimas tai būtų tik į naudą, bet, deja, šią formą egzaminai galios ne tik 2018 m., bet ir vėlesniuose. Kad moksleiviams nereikėtų skųstis sunkumu ugdymo procesas, tačiau turėtumėte greitai imtis vadovėlių ir atlikti testų demonstracines versijas, kad praplėstumėte savo žinių akiratį ir atvyktumėte visiškai apsiginklavę.
Noriu pastebėti, kad tėvų dalyvavimas vaidina didžiulį vaidmenį ruošiant mokinius egzaminams. Jei mamos ir tėčiai pasirūpina, kad jų vaikas gautų viską, kas yra naujausia metodologinius pokyčius ir išmokas, o taip pat kreiptis pagalbos į dėstytojus, tuomet nekyla abejonių, kad vaikas su šiuo išbandymu susidoros be didelių sunkumų.
Pasiruošimo metu reikia nepamiršti, kad FIPI periodiškai atlieka KIM pakeitimus, kurie padeda padidinti 9 klasės mokinių žinių patikrinimo objektyvumą ir išsamumą.
Apie visas naujoves ir subtilybes vykdant OGE galite sužinoti „Roskomnadzor“ svetainėje, kur naujienos greitai paskelbiamos ir prieinamos kiekvienam vartotojui internete.
Kas yra OGE?
Norėdami suprasti, ko tikėtis iš šio egzamino, turite suprasti jo esmę. Minėtos santrumpos nereikėtų painioti su valstybiniu baigiamuoju pažymėjimu (GIA), su kuriuo susiduria ir baigiantys vidurinę mokyklą.
OGE yra sertifikavimo dalis ir pagrindinė grandis. Tai išbandymas, kurį atlieka dauguma rusiškų mokyklų devintokų. Kaip ir vieningas valstybinis egzaminas, taip ir šis egzaminas vyksta tam tikromis dienomis ir jį kontroliuoja specialiai sukurtų komisijų nariai.

Be OGE, valst galutinis sertifikatas apima GVE arba valstiją baigiamasis egzaminas. Jį dažniausiai imasi ugdymo įstaigų studentai uždaro tipo, būtent nepilnamečių nusikaltėlių kolonijose, internatinėse mokyklose. Studentai taip pat priima GVE užsienio institucijos, taip pat neįgaliems vaikams.
Planuojami OGE pakeitimai 2018 m
Būsimos OGE naujovės yra skirtos tobulinti egzaminų procesą ir atrodo taip:
- Už egzaminą gauti pažymiai turės įtakos pažymėjimui.
- Įvedama bendra balų skalė su bendra minimalia riba visiems.
- KIM yra vienodi visiems šalies regionams, t.y. jų galimybės bus kuriamos ne atskirai pagal regionus, o federaliniu lygiu.

- Informatikos egzaminas bus laikomas asmeniniu kompiuteriu.
- Jei per egzaminą studentas iš trijų ar keturių dalykų gavo „Nepavyko“, tai OGE perlaikyti bus galima tik kitais metais, t.y. vaikas paliekamas antriems metams.
- Kai kuriuose regionuose jie planuoja pristatyti egzaminas žodžiu rusų kalba.
Kalbant apie padidėjimą privalomi dalykai, tada tai neįvyks 2018 m. Kaip ir anksčiau, OGE bus du privalomos disciplinos(matematika ir rusų kalba), taip pat bus įtraukti du dalykai, iš kurių galima rinktis. Pareigūnai šią naujovę priėmė remdamiesi tuo, kad tik dviejų disciplinų testavimas neleidžia praplėsti studento akiračio.
Be to, papildomų elementų išlaikęs egzaminą padės mokiniui patekti į mokymo įstaigas (ar klases) su specialiu dėmesiu.

Tie, kurie dalyvaus OGE 2018 m., Jau gali susipažinti visas sąrašas Galima rinktis prekes:
- Literatūra
- Fizika
- Biologija
- Geografija
- Socialinis mokslas
- Istorija
- Užsienio kalbos
- Informatika
Kaip OGE gali paveikti sertifikatą?

Nuo 2018 metų valstybinio egzamino išlaikymo rezultatai turės įtakos galutiniam pažymiui pažymėjime. Tai yra, studentas gali padidinti arba padidinti savo balą. Pasirodo, jei per visus mokslo metus mokinys „nepadarė“ tam tikro dalyko, bet OGE jį parašė „Puikiai“, tada vietoj „4“ dokumente bus įrašytas „5“.
OGE tvarkaraštis 2018 m
Visai kaip Vienintelis valstybinis egzaminas, OGE devintokams skirstomas į tris laikotarpius: ankstyvąjį, pagrindinį ir papildomą. Datos jau žinomos ir jas galite peržiūrėti jau dabar.
Ar įmanoma „apgauti“ per egzaminą?

Praėjusiais metais į internetą nutekėjus visų valstybinių egzaminų atsakymams, jie nusprendė gerokai pagerinti pasirinkimų apsaugą. Daugelyje taškų, kur atliekamas žinių patikrinimas, įrengiamos vaizdo kameros ir metalo detektoriai.
Tačiau yra drąsių sielų, kurios sugeba į egzaminą atsinešti popierinius sukčiavimo lapus. Nors sėkme per daug pasikliauti nereikia, nes bet kurią akimirką gali būti pastebėtas. Geriau tinkamai pasiruošti prieš egzaminą ir jau jo metu, mikliai panaudojant žinias, oriai susidoroti su visomis užduotimis.









